-
Die
vorliegende Erfindung betrifft die Verwendung von α-Aminosäurederivaten
zur Löslichkeitsverbesserung von schwerlöslichen
Substanzen in Wasser oder wässrigen Lösungen,
sowie Mischungen und bevorzugte Zubereitungen.
-
Wirkstoffe
sind Substanzen, die – in relativ kleinen Mengen vorkommend
oder zugeführt – große physiologische
Wirkung entfalten können. Sie sind aus unserem heutigen
Alltag nicht mehr wegzudenken und spielen beispielsweise sowohl
in der Schönheitspflege wie auch in der Heilbehandlung
und der Nahrungsaufnahme eine wichtige Rolle.
-
Es
ist bekannt, dass die ausreichende Löslichkeit von Wirkstoffen
in nicht-festen Zubereitungen wie z. B. Emulsionen hinsichtlich
des Wirkpotentials der Substanz sowie hinsichtlich der galenischen
Akzeptanz der Zubereitung von großer Bedeutung ist.
-
Für
eine Reihe von schwerlöslichen Komponenten ist bekannt,
dass sie eine ausreichende Löslichkeit in der Zubereitung
ohne Rekristallisationseffekte nur schwer erzielen.
-
Es
ist bekannt, dass insbesondere der Einsatz von Naturstoffen oder
naturidentischen Stoffen, wie z. B. Bioflavonoiden, Chromonen, Chromanonen,
Coumarinen und Coumaranonen, durch deren mangelnde Löslichkeit
erheblich limitiert sein kann. Des Weiteren kann eine zu geringe
Löslichkeit auch für zahlreiche synthetische Komponenten
einen erheblichen Mangel darstellen. Als Beispiele hierfür
sind ausgewählte Kosmetikwirkstoffe, wie z. B. UV-Filter,
Antioxidantien, Selbstbräunungs-/Hautaufhellungswirkstoffe,
Anti-Aging-Wirkstoffe zu nennen.
-
Erstrebenswert
ist es daher, Zubereitungen zu entwickeln, die diesen Mangel beseitigen.
Dabei sollen keine Alternativmängel erzeugt werden, wie
dies beispielsweise durch den Einsatz unerwünschter Sekundärkomponenten,
wie z. B. Lösevermittler, der Fall ist.
-
Eine
weitere Schwierigkeit bei der Herstellung von Kosmetika besteht
darin, dass Wirkstoffe, die in kosmetische Zubereitungen eingearbeitet
werden sollen, oft keine ausreichende Löslichkeit im sauren
pH-Bereich aufweisen.
-
Beispielsweise
muss Eusolex® 232 (Phenylbenzimidazolsulfonsäure,
2-Phenylbenzimidazol-5-sulfonsäure, PBSA) zur Verwendung
in Kosmetikprodukten leicht alkalisiert werden, um eine ausreichende
Löslichkeit zu erzielen. Nachteilig dabei ist der erforderliche
alkalische pH-Wert der Rezeptur von pH 7 bis 8. Demgegenüber
sind saure Kosmetika aus Gründen der Verträglichkeit
und des natürlich-sauren pH-Wertes der Haut bevorzugt.
Im sauren Bereich können viele Wirkstoffe, beispielsweise
PSBA, aber bisher nicht verwendet werden, da es hier zur Rekristallisation
der Sulfonsäure kommt. Der Idealwert einer kosmetischen
Rezeptur liegt bei pH 5,5 und entspricht somit dem natürlichen
pH-Wert der Haut.
-
Es
besteht daher Bedarf nach hautverträglichen Lösevermittlern,
die sich auch zum Einsatz in hautpflegenden, kosmetischen und dermatologischen
Zubereitungen eignen.
-
Aufgabe
der vorliegenden Erfindung ist es daher, Verbindungen zur Verfügung
zu stellen, deren Verwendung die Löslichkeit von Substanzen
verbessert, die in Wasser schwerlöslich sind, wenn der
pH-Wert der Lösung unter pH 7 liegt.
-
Überraschend
wurde dabei gefunden, dass sich Derivate von α-Aminosäuren
hervorragend zur Löslichkeitssteigerung schwerlöslicher
Substanzen, wie zuvor definiert, eignen.
-
Ein
erster Gegenstand der vorliegenden Erfindung ist daher die Verwendung
von mindestens einem α-Aminosäurederivat, dessen
Salz oder Hydrat zur Löslichkeitsverbesserung von einer
oder mehreren schwerlöslichen Substanzen in Wasser oder
wässrigen Lösungen. Dabei ist das α-Stickstoffatom
des mindestens einen α-Aminosäurederivates quatemär,
tertiär oder sekundär.
-
Als
schwerlösliche Substanzen im Sinne dieser Erfindung werden
insbesondere Substanzen angesehen, deren Löslichkeit in
Wasser bei einer Temperatur zwischen 20° und 25°C
unter 1 Gew.-% liegt, wenn der pH-Wert der Lösung unter
pH 7 liegt.
-
Bevorzugt
wird bei der erfindungsgemäßen Verwendung daher
die Löslichkeit einer Substanz verbessert, deren Löslichkeit
in Wasser bei Abwesenheit des α-Aminosäurederivates
bei einer Temperatur zwischen 20° und 25°C und
bei einem pH-Wert der Zubereitung zwischen 3 und 6,5 kleiner als
1 Gew.-% ist.
-
Vorteile
der erfindungsgemäßen Verwendung sind insbesondere
die gute Hautverträglichkeit sowie die Tatsache, das durch
die erfindungsgemäße Verwendung des α-Aminosäurederivates
eine Möglichkeit gegeben ist, Wirkstoffe, die nur im alkalischen
Bereich eine ausreichende Löslichkeit aufweisen, auch in
sauren oder neutralen kosmetischen und dermatologischen Zubereitungen
zu verwenden.
-
Der
Begriff ausreichende Löslichkeit in Sinne dieser Erfindung
umschreibt die Eigenschaft eines Stoffes, bei produktspezifischer
Lagerung nicht auszukristallisieren. Als ausreichende Löslichkeit
wird je nach Anwendung insbesondere eine Löslichkeit erachtet,
die eine gute Wirksamkeit bei gleichzeitiger Lagerstabilität gewährt.
-
Gute
Wirksamkeiten werden erzielt, wenn ausreichend Wirkstoff in der
Formulierung gelöst werden kann und im Verlauf der Lagerung
auch gelöst bleibt, d. h. in diesem Fall nicht wieder auskristallisiert.
-
Bevorzugt
wird bei der erfindungsgemäßen Verwendung als
mindestens ein α-Aminosäurederivat ein nicht-amphotensidisches
Betain, 2-Pyrrolidon-5-carbonsäure und/oder ein Derivat
des Formiminoglycins verwendet.
-
Ganz
allgemein umfasst der Begriff Betain alle Verbindungen, die eine
quaternäre Ammoniumgruppe und einen Säurerest
enthalten. Ohne Einschränkung der Allgemeinheit wird als
nicht-amphotensidisches Betain erfindungsgemäß besonders
bevorzugt Trimethylglycin verwendet.
-
Als
weiteres α-Aminosäurederivat wird besonders bevorzugt
die 2-Pyrrolidon-5-carbonsäure verwendet:
-
Ohne
Einschränkung der Allgemeinheit wird als Derivat des Formiminoglycin
erfindungsgemäß besonders bevorzugt eine oder
mehrere der folgenden Verbindungen verwendet:
-
Ganz
besonders bevorzugt wird Kreatinin als Formiminoglycin erfindungsgemäß verwendet.
-
Sämtliche α-Aminosäurederivate
können erfindungsgemäß auch in Form ihrer
Salze oder Hydrate Verwendung finden, beispielsweise das Kreatinhydrat.
-
Bevorzugt
wird erfindungsgemäß die Löslichkeit
einer schwerlöslichen Substanz verbessert, die ausgewählt
ist aus der Gruppe Chromone, Chromanone, Flavonoide und aromatischen
Monosulfonsäuren.
-
Unter
Chromon-Derivaten werden vorzugsweise bestimmte Chromen-on-Derivate,
die sich als Wirkstoffe zur vorbeugenden Behandlung von menschlicher
Haut und menschlicher Haare gegen Alterungsprozesse und schädigende
Umwelteinflüssen eignen, verstanden. Sie zeigen gleichzeitig
ein niedriges Irritationspotential für die Haut, beeinflussen
die Wasserbindung in der Haut positiv, erhalten oder erhöhen
die Elastizität der Haut und fördern somit eine
Glättung der Haut.
-
Ohne
Einschränkung der Allgemeinheit handelt es sich bei dem
schwerlöslichen Chromen-on, dessen Löslichkeit
erfindungsgemäß verbessert wird, besonders bevorzugt
um eine Verbindung der allgemeinen Formel (I)
wobei
R
1 und
R
2 gleich oder verschieden sein können
und steht für H, geradkettige oder verzweigte C
1- bis C
20-Alkylgruppen
oder geradkettige oder verzweigte C
1- bis
C
20-Hydroxyalkyl-gruppen
R
3 steht
für H oder geradkettige oder verzweigte C
1-
bis C
20-Alkylgruppen,
R
4 steht
für H oder OR
7,
R
5 und
R
6 gleich oder verschieden sein können
und steht für H, OH oder geradkettige oder verzweigte C
3- bis C
20-Alkenyl-gruppen,
R
7 steht für H oder geradkettige
oder verzweigte C
1- bis C
20-Alkylgruppen,
wobei
mindestens zwei der Substituenten R
1, R
2, R
4 bis R
6 verschieden von H sind.
-
Unter
den Chromonderivaten der Formel (I) ist 5,7-Dihydroxy-2-methylchromon
besonders bevorzugt.
-
Unter
Chromanon-Derivaten werden vorzugsweise bestimmte Chroman-on-Derivate,
die sich als Wirkstoffe zur Pflege, Konservierung oder Verbesserung
des allgemeinen Zustandes der Haut oder Haare und zur Prophylaxe
gegen zeit- und/oder lichtinduzierte Alterungsprozesse der menschlichen
Haut oder menschlicher Haare und zur Prophylaxe und/oder Behandlung
von Hautkrankheiten eignen, verstanden. Sie zeigen gleichzeitig
ein niedriges Irritationspotential für die Haut, beeinflussen
die Wasserbindung in der Haut positiv, erhalten oder erhöhen
die Elastizität der Haut und fördern somit eine
Glättung der Haut.
-
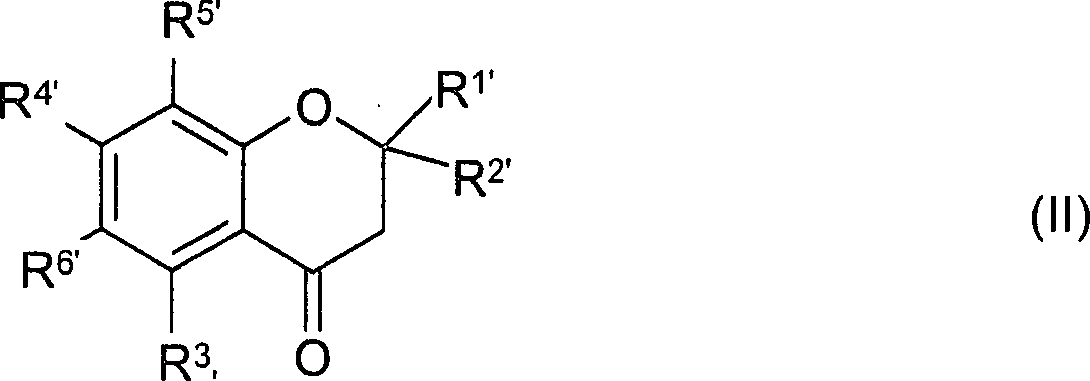
Ohne
Einschränkung der Allgemeinheit handelt es sich bei der
schwerlöslichen Substanz, deren Löslichkeit erfindungsgemäß verbessert
wird, besonders bevorzugt um eine Verbindung der allgemeinen Formel (II)
wobei
R
1' und
R
2' gleich oder verschieden sein können
und ausgewählt sind aus
- – H,
- – geradkettigen oder verzweigten C1-
bis C20-Alkylgruppen,
- – geradkettigen oder verzweigten C3-
bis C20-Alkenylgruppen,
- – geradkettigen oder verzweigten C1-
bis C20-Hydroxyalkylgruppen,
- – C3- bis C10-Cycloalkylgruppen
und/oder C3- bis C12-Cycloalkenylgruppen,
wobei die Ringe jeweils auch durch -(CH2)n-Gruppen mit n = 1 bis 3 überbrückt
sein können
oder R1' und R2' durch (CH2)o verbunden sind, wobei 0 für 0,
1, 2, 3, 4, 5 oder 6 steht,
R3', R4' und R5' jeweils
unabhängig voneinander ausgewählt sind aus
- – H, OH,
- – geradkettigen oder verzweigten C1-
bis C20-Alkoxygruppen,
- – geradkettigen oder verzweigten C1-
bis C20-Acyloxygruppen,
- – geradkettigen oder verzweigten C1-
bis C20-Alkylgruppen,
- – geradkettigen oder verzweigten C3-
bis C20-Alkenylgruppen,
- – geradkettigen oder verzweigten C1-
bis C20-Hydroxyalkylgruppen, und
R6' steht für H, OH, COOH, COCH3,
- – geradkettigen oder verzweigten C1-
bis C20-Alkylgruppen,
- – geradkettigen oder verzweigten C3-
bis C20-Alkenylgruppen,
- – geradkettigen oder verzweigten C1-
bis C20-Hydroxyalkylgruppen,
- – geradkettigen oder verzweigten C1-
bis C20-Alkoxygruppen,
- – geradkettigen oder verzweigten C1-
bis C20-Alkylgruppen,
- – geradkettigen oder verzweigten C1-
bis C20-Alkoxycarbonylgruppen, oder geradkettigen
oder verzweigten C1- bis C20-Acyloxygruppen.
-
Der
Anteil an einer oder mehreren Verbindungen ausgewählt aus
Chromon- oder Chromanon-Derivaten in einer Zubereitung beträgt
vorzugsweise von 0,001 Gew.-% bis 5 Gew.-%, besonders bevorzugt
von 0,01 Gew.-% bis 2 Gew.-%, bezogen auf die gesamte Zubereitung.
-
Als
Flavonoide werden erfindungsgemäß die Glykoside
von Flavanonen, Flavonen, 3-Hydroxyflavonen (= Flavonolen), Auronen,
Isoflavonen und Rotenoiden aufgefasst [Römpp Chemie Lexikon,
Band 9, 1993]. Im Rahmen der vorliegenden Erfindung werden hierunter
jedoch auch die Aglykone, d. h. die zuckerfreien Bestandteile, und
die Derivate der Flavonoide und der Aglykone verstanden. Weiterhin
wird im Rahmen der vorliegenden Erfindung unter dem Begriff Flavonoid
auch Anthocyanidin (Cyanidin) verstanden.
-
Die
Verwendung von Flavonoiden insbesondere in der Kosmetik bzw. Pharmazie
ist an sich bekannt. Flavonoide sind im allgemeinen schwerlösliche
Verbindungen, mit Ausnahme von beispielsweise Troxerutin und α-Glucosylrutin.
-
Ohne
Einschränkung der Allgemeinheit handelt es sich bei der
schwerlöslichen Substanz, dessen Löslichkeit erfindungsgemäß verbessert
wird, besonders bevorzugt um Isoquercetin oder eine Verbindung der
allgemeinen Formel (III)
wobei
R
8,
R
9 und R
10 gleich
oder verschieden sein können und jeweils unabhängig
voneinander für OH, CH
3COO, Alkoxy-
oder Monoglykosid-Reste stehen, wobei die Alkoxy-Reste verzweigt
und unverzweigt sein und 1 bis 8 C-Atome aufweisen können,
R
11 ein Mono- oder Diglykosid-Rest ist, wobei
an diesen Glykosid-Rest jeweils über eine Gruppe -O-
R
12 die
Bedeutung der Reste R
8 bis R
10 besitzt,
und wobei ein oder mehrere Wasserstoffatome in den OH-Gruppen des
oder der Glykosid-Reste jeweils unabhängig voneinander
auch durch Acetyl- oder durch Alkyl-Reste mit 1 bis 8 C-Atomen ersetzt
sein können. Unter den Verbindungen der Formel (III) ist
Tilirosid besonders bevorzugt.
-
Bevorzugt
wird das mindestens eine Flavonoid, wie zuvor beschrieben, für
die erfindungsgemäße Verwendung in entsprechenden
Formulierungen in einer Gesamtmenge von 0,01 Gew.-% bis 10 Gew.-%,
noch bevorzugter in einer Menge von 0,1 Gew.-% bis 5 Gew.-% eingesetzt.
-
Aromatische
Monosulfonsäuren sind Wirkstoffe, die sich unter anderem
als UV-Filter insbesondere in der Kosmetik bzw. Pharmazie eignen.
Ihre Verwendung in kosmetischen und dermatologischen Zubereitungen ist
bekannt.
-
Ohne
Einschränkung der Allgemeinheit handelt es sich bei der
aromatischen Monosulfonsäure, deren Löslichkeit
erfindungsgemäß verbessert wird, besonders bevorzugt
um nur im Alkalischen wasserlösliche UV-Filter, ausgewählt
aus der Gruppe 2-Arylbenzimidazol-5-sulfonsäuren, 2-Hydroxy-4-methoxybenzophenon-5-sulfonsäure
oder Sulfonsäure-Derivate des 3-Benzylidencamphers.
2-Hydroxy-4-methoxybenzophenon-5-sulfonsäure;
Arylbenzimidazolsulfonsäuren
entsprechen beispielsweise bevorzugt der allgemeinen Formel (IV)
wobei Ar für unsubstituiertes
oder durch eine oder mehrere C
1- bis C
6-Alkyl- oder Alkoxygruppen substituiertes Phenyl
steht.
-
Unter
den Verbindungen der Formel IV ist 2-Phenylbenzimidazol-5-sulfonsäure
besonders bevorzugt.
2-Phenylbenzimidazol-5-sulfonsäure.
-
Monosulfonsäure-Derivate
des 3-Benzylidencamphers sind beispielsweise 4-(2-Oxo-3-bornylidenmethyl)benzolsulfonsäure
oder 2-Methyl-5-(oxo-3-bornylidenmethyl)benzolsulfonsäure.
4-(2-Oxo-3-bornylidenmethyl)benzolsulfonsäure;
3-Methyl-5-[4,7,7-trimethyl-3-oxo-bicyclo[2.2.1]hept-(2Z)-ylidenemethyl]-benzolsulfonsäure.
-
Ohne
Einschränkung der Allgemeinheit wird beispielsweise die
Löslichkeit von Tilirosid, 5,7-Dihydroxy-2-methyl-chromen-4-on
oder Eusolex® 232 (2-Phenylbenzimidazol-5-sulfonsäure)
in Wasser oder einer wässrigen Lösung durch die
Verwendung von 2-Pyrrolidon-5-carbonsäure, Ectoin, Hydroxyectoin,
Kreatin oder Kreatinin verbessert.
-
Eine
bevorzugte wässrige Lösung ist beispielsweise
ein Gemisch aus Wasser und einem Alkohol, wie Methanol, Ethanol
oder Propanol, besonders bevorzugt Ethanol. Das Gewichtsverhältnis
Alkohol zu Wasser ist bevorzugt zwischen 10:1 und 1:100, besonders
bevorzugt sind Gewichtsverhältnisse zwischen 5:1 und 1:50.
Es sind jedoch auch Ausführungsformen von wässrigen
Lösungen bevorzugt, die keinen Alkohol enthalten. In solchen
wässrigen Lösungen wird die Löslichkeit
von aromatischen Monsulfonsäuren besonders bevorzugt verbessert.
-
Ein
weiterer Gegenstand der vorliegenden Erfindung sind Zubereitungen,
bevorzugt kosmetische Mittel, pharmazeutische Mittel oder Lebensmittel,
die mindestens ein α-Aminosäurederivat und mindestens
eine schwerlösliche Substanz, wie zuvor definiert, enthalten,
wobei der Anteil des α- Aminosäurederivats in Gewichtsprozent
größer ist als der Anteil der schwerlöslichen
Substanz in Gewichtsprozent, bezogen auf die Zubereitung.
-
In
einer Ausführungsform sind Zubereitungen bevorzugt, bei
denen das α-Aminosäurederivat gewählt wird
aus 2-Pyrrolidon-5-carbonsäure, Kreatinin, Kreatin, Ectoin
und Hydroxyectoin, ganz besonders bevorzugt wird Kreatinin gewählt.
Weiterhin sind Zubereitungen bevorzugt, in denen die schwerlösliche
Substanz eine aromatische Monosulfonsäure ist.
-
In
einer bevorzugten Ausführungsform der erfindungsgemäßen
Zubereltung ist das mindestens eine α-Aminosäurederivat
in einer Menge von 0,05 Gew.-% bis 20 Gew.-%, bevorzugt in einer
Menge von 0,5 Gew.-% bis 10 Gew.-% und besonders bevorzugt in einer
Menge von 1 Gew.-% bis 5 Gew.-%, enthalten.
-
In
einer weiteren bevorzugten Ausführungsform einer Zubereitung
sind das mindestens eine α-Aminosäurederivat und
die mindestens eine aromatische Monosulfonsäure in einem
Gewichtsprozentverhältnis von 10:1 bis 1,1:1, bevorzugt
von 5:1 bis 1,5:1 enthalten, ganz besonders bevorzugt von 3:1 bis
2:1.
-
Ein
Vorteil dieser erfindungsgemäßen Zubereitung ist,
dass dabei der pH-Wert der wässrigen Phase der Zubereitung
kleiner 7, bevorzugt kleiner 6,5, ist.
-
Bei
den Zubereitungen handelt es sich dabei üblicherweise um
topisch anwendbare Zubereitungen, beispielsweise kosmetische oder
dermatologische Formulierungen. Die Zubereitungen enthalten in diesem Fall
einen kosmetisch oder dermatologisch geeigneten Träger
und je nach gewünschtem Eigenschaftsprofil optional weitere
geeignete Inhaltsstoffe. Handelt es sich um pharmazeutische Zubereitungen,
so enthalten die Zubereitungen in diesem Fall einen pharmazeutisch
verträglichen Träger und optional weitere pharmazeutische
Wirkstoffe. Handelt es sich um Nahrungsergänzungsmittel,
so ist ein dafür geeigneter Träger auszuwählen.
-
Handelt
es sich bei den Zubereitungen um Parfums, so ist es in einer Erfindungsvariante
bevorzugt, wenn neben den Duftstoffen oder Parfümölen
und den Flavonoiden und typischen Trägersubstanzen, wie Wasser,
Lösungsmitteln, wie Alkohole, Ölen und ggf. Emulgatoren
keine weiteren Hilfsmittel enthalten sind.
-
Im
Sinne der vorliegenden Erfindung wird neben dem Begriff Zubereitung
gleichbedeutend auch der Begriff Mittel oder Formulierung verwendet.
-
Alle
Verbindungen oder Komponenten, die in den Zubereitungen verwendet
werden können, sind entweder bekannt und käuflich
erwerbbar oder können nach bekannten Verfahren synthetisiert
werden.
-
Ein
weiterer Gegenstand der vorliegenden Erfindung ist eine Mischung,
insbesondere eine Feststoffmischung, die mindestens ein α-Aminosäurederivat,
bevorzugt ausgewählt aus 2-Pyrrolidon-5-carbonsäure, Kreatinin,
Kreatin, Ectoin und Hydroxyectoin, und mindestens eine schwerlösliche
Substanz, bevorzugt ausgewählt aus Chromonen, Chromanonen,
Flavonoiden und aromatischen Monosulfonsäuren enthält.
Diese Mischung ist insbesondere geeignet zur Herstellung einer kosmetischen,
pharmazeutischen Zubereitung oder Lebensmittelzubereitung.
-
In
einer bevorzugten Ausführungsform der erfindungsgemäßen
Mischung sind das mindestens eine α-Aminosäurederivat
und die mindestens eine schwerlösliche Substanz in einem
Gewichtsprozentverhältnis von 10:1 bis 1,1:1, bevorzugt
von 5:1 bis 1,5:1 enthalten, ganz besonders bevorzugt von 3:1 bis
2:1. enthalten.
-
In
einer weiteren bevorzugten Ausführungsform enthält
die erfindungsgemäße Mischung 90 Gew.-% bis 11
Gew.-% an mindestens einem α-Aminosäurederivat,
wie zuvor definiert, und 45 Gew.-% bis 10 Gew.-% an mindestens einer
schwerlöslichen Substanz, wie zuvor definiert. Neben den
beiden Hauptkomponenten, wie zuvor definiert, kann die Mischung
zudem weitere Substanzen enthalten, wie beispielsweise Trennmittel. Als
Trennmittel können beispielsweise Kieselsäure
(Aerosile), Talk, Zinkoxid oder Stärke eingesetzt werden.
-
Ganz
besonders bevorzugt ist die schwerlösliche Substanz eine
aromatische Monosulfonsäure, vorzugsweise ausgewählt
aus der Gruppe 2-Arylbenzimidazol-5-sulfonsäuren der Formel
IV, wie zuvor beschrieben, 2-Hydroxy-4-methoxybenzophenon-5-sulfonsäure
oder Derivate des 3-Benzylidencamphers. Besonders bevorzugt wird
2-Phenyl-benzimidazol-5-sulfonsäure ausgewählt.
-
Weitere
bevorzugte Kombinationen von Ausführungsformen sind in
den Ansprüchen offenbart.
-
Die
erfindungsgemäßen Mischungen können dabei
mit Hilfe von Techniken hergestellt werden, die dem Fachmann wohl
bekannt sind. Beispielsweise wird das α-Aminosäurederivat
in einem geeigneten Lösungsmittel gelöst, bevorzugt
in Wasser oder einer wässrigen Lösung, die schwerlösliche
Substanz wird eingetragen und das Lösungsmittel wieder
mit einer geeigneten Technik entfernt. Geeignet ist beispielsweise
eine Destillation oder Gefriertrocknung.
-
Ein
weiterer Gegenstand der Erfindung ist daher auch ein Verfahren zur
Herstellung einer Mischung, wie zuvor beschrieben, dadurch gekennzeichnet,
dass ein α-Aminosäurederivat in einem geeigneten
Lösungsmittel gelöst wird, die schwerlösliche
Substanz und gegebenenfalls ein Trennmittel eingetragen wird und
das Lösungsmittel entfernt wird.
-
Die
Zubereitungen oder Mischungen können die genannten notwendigen
oder optionalen Bestandteile umfassen oder enthalten, daraus im
wesentlichen oder daraus bestehen.
-
In
den beschriebenen Zubereitungen und Mischungen, die erfindungsgemäß mindestens
ein Derivat einer α-Aminosäure und mindestens
eine schwerlösliche Substanz enthalten, können
weiterhin auch Pigmente enthalten sein, wobei der Schichtaufbau
der Pigmente nicht limitiert ist.
-
Vorzugsweise
sollte das Farbpigment bei Einssatz von 0,5 Gew.-% bis 5 Gew.-%
hautfarben oder bräunlich sein. Die Auswahl eines entsprechenden
Pigments ist für den Fachmann geläufig.
-
Vorteilhafte
Farbpigmente sind beispielsweise Titandioxid, Glimmer, Eisenoxide
(z. B. Fe2O3, Fe3O4, FeO(OH)) und/oder
Zinnoxid. Vorteilhafte Farbstoffe sind beispielsweise Carmin, Berliner
Blau, Chromoxidgrün, Ultramerinblau und/oder Manganviolett.
-
Es
ist insbesondere vorteilhaft, die Farbstoffe und/oder Farbpigmente
aus der folgenden Liste zu wählen. Die Colour Index Nummern
(CIN) sind dem Rowe Colour Index, 3. Auflage, Society of Dyers and
Colourists, Bradford, England, 1971 entnommen.
| Chemische
oder sonstige Bezeichnung | CIN | Farbe |
| Pigment
Green | 10006 | grün |
| Acid
Green 1 | 10020 | Grün |
| 2,4-Dinitrohydroxynaphthalin-7-sulfonsäure | 10316 | Gelb |
| Pigment
Yellow 1 | 11680 | Gelb |
| Pigment
Yellow 3 | 11710 | Gelb |
| Pigment
Orange 1 | 11725 | Orange |
| 2,4-Dihydroxyazobenzol | 11920 | Orange |
| Solvent
Red 3 | 12010 | Rot |
| 1-(2'-Chlor-4'-nitro-1'-phenylazo)-2-hydroxynaphthalin | 12085 | Rot |
| Pigment
Red 3 | 12120 | Rot |
| Ceresrot;
Sudanrot; Fettrot G | 12150 | Rot |
| Pigment
Red 112 | 12370 | Rot |
| Pigment
Red 7 | 12420 | Rot |
| Pigment
Brown 1 | 12480 | Braun |
| 4-(2'-Methoxy-5'sulfonsäurediethylamid-1'-phenylazo)-3-hydroxy-5''-chloro-2'',4''-dimethoxy2-naphthoesäureanilid | 12490 | Rot |
| Disperse
Yellow 16 | 12700 | Gelb |
| 1-(4-Sulfo-1-phenylazo)-4-amino-benzol-5-sulfosäure | 13015 | Gelb |
| 2,4-Dihydroxy-azobenzol-4'-sulfosäure | 14270 | Orange |
| 2-(2,4-Dimethylphenylazo-5-sulfosäure)-1-hydroxynaphthalin-4-sulfosäure | 14700 | Rot |
| 2-(4-Sulfo-1-naphthylazo)-1-naphthol-4-sulfosäure | 14720 | Rot |
| 2-(6-Sulfo-2,4-xylylazo)-1-naphthol-5-sulfosäure | 14815 | Rot |
| 1-(4'-Sulfophenylazo)-2-hydroxynaphthalin | 15510 | Orange |
| 1-(2-Sulfosäure-4-chlor-5-carbonsäure-1-phenylazo)-2-hydroxynaphthalin | 15525 | Rot |
| 1-(3-Methyl-phenylazo-4-sulfosäure)-2-hydroxynaphthalin | 15580 | Rot |
| 1-(4',(8')-Sulfosäurenaphthylazo)-2-hydroxynaphthalin | 15620 | Rot |
| 2-Hydroxy-1,2'-azonaphthalin-1'-sulfosäure | 15630 | Rot |
| 3-Hydroxy-4-phenylazo-2-naphthylcarbonsäure | 15800 | Rot |
| Chemische
oder sonstige Bezeichnung | CIN | Farbe |
| 1-(2-Sulfo-4-methyl-1-phenylazo)-2-naphthylcarbonsäure | 15850 | rot |
| 1-(2-Sulfo-4-methyl-5-chlor-1-phenylazo)-2-hydroxy-naphthalin-3-carbonsäure | 15865 | Rot |
| 1-(2-Sulfo-1-naphthylazo)-2-hydroxynaphthalin-3-carbonsäure | 15880 | Rot |
| 1-(3-Sulfo-1-phenylazo)-2-naphthol-6-sulfosäure | 15980 | Orange |
| 1-(4-Sulfo-1-phenylazo)-2-naphthol-6-sulfosäure | 15985 | Gelb |
| Allura
Red | 16035 | Rot |
| 1-(4-Sulfo-1-naphthylazo)-2-naphthol-3,6-disulfosäure | 16185 | Rot |
| Acid
Orange 10 | 16230 | Orange |
| 1-(4-Sulfo-1-naphthylazo)-2-naphthol-6,8-disulfosäure | 16255 | Rot |
| 1-(4-Sulfo-1-naphthylazo)-2-naphthol-3,6,8-trisulfosäure | 16290 | Rot |
| 8-Amino-2-phenylazo-1-naphthol-3,6-disulfosäure | 17200 | Rot |
| Acid
Red 1 | 18050 | Rot |
| Acid
Red 155 | 18130 | Rot |
| Acid
Yellow 121 | 18690 | Gelb |
| Acid
Red 180 | 18736 | Rot |
| Acid
Yellow 11 | 18820 | Gelb |
| Acid
Yellow 17 | 18965 | Gelb |
| 4-(4-Sulfo-1-phenylazo)-1-(4-sulfophenyl)-5-hydroxy-pyrazolon-3-carbonsäure | 19140 | Gelb |
| Pigment
Yellow 16 | 20040 | Gelb |
| 2,6-(4'-Sulfo-2'',4''-dimethyl)-bis-phenylazo)1,3-dihydroxybenzol | 20170 | Orange |
| Acid
Black 1 | 20470 | Schwarz |
| Pigment
Yellow 13 | 21100 | Gelb |
| Pigment
Yellow 83 | 21108 | Gelb |
| Solvent
Yellow | 21230 | Gelb |
| Acid
Red 163 | 24790 | Rot |
| Acid
Red 73 | 27290 | Rot |
| 2-[4'-(4''-Sulfo-1''-phenylazo)-7'-sulfo-1'-naphthylazo]-1-hydroxy-7-aminonaphthalin-3,6-disulfosäure | 27755 | schwarz |
| Chemische
oder sonstige Bezeichnung | CIN | Farbe |
| 4-[4''-Sulfo-1''-phenylazo)-7'-sulfo-1'-naphthylazo]-1-hydroxy-8-acetyl-aminonaphthalin-3,5-disulfosäure | 28440 | Schwarz |
| Direct
Orange 34, 39, 44, 46, 60 | 40215 | Orange |
| Food
Yellow | 40800 | Orange |
| trans-β-Apo-8'-Carotinaldehyd
(C30) | 40820 | Orange |
| trans-Apo-8'-Carotinsäure
(C30)-ethylester | 40850 | Orange |
| Canthaxanthin | 40850 | Orange |
| Acid
Blue 1 | 42045 | Blau |
| 2,4-Disulfo-5-hydroxy-4'-4''-bis-(diethylamino)triphenyl-carbinol | 42051 | Blau |
| 4-[(-4-N-Ethyl-p-sulfobenzylamino)-phenyl-(4-hydroxy-2-sulfophenyl)-(methylen)-1-(N-ethylN-p-sulfobenzyl)-2,5-cyclohexadienimin] | 42053 | Grün |
| Acid
Blue 7 | 42080 | Blau |
| (N-Ethyl-p-sulfobenzyl-amino)-phenyl-(2-sulfophenyl)-methylen-(N-ethyl-N-p-sulfo-benzyl) Δ2,5-cyclohexadienimin | 42090 | Blau |
| Acid
Green 9 | 42100 | Grün |
| Diethyl-di-sulfobenzyl-di-4-amino-2-chlor-di-2-methyl-fuchsonimmonium | 42170 | Grün |
| Basic
Violet 14 | 42510 | Violet |
| Basic
Violet 2 | 42520 | Violet |
| 2'-Methyl-4'-(N-ethyl-N-m-sulfobenzyl)-amino-4''-(N-diethyl)-aminn-2-methyl-N-ethyllN-m-sulfobenzyl-fuchsonimmonium | 42735 | Blau |
| 4'-(N-Dimethyl)-amino-4''-(N-phenyl)-aminonaphtho-N-dimethylfuchsonimmonium | 44045 | Blau |
| 2-Hydroxy-3,6-disulfo-4,4'-bis-dimethylaminonaphthofuchsonimmonium | 44090 | Grün |
| Acid
Red 52 | 45100 | Rot |
| 3-(2'-Methylphenylamino)-6-(2'-methyl-4'-sulfophenylamino)-9-(2''-carboxyphenyl)-xantheniumsalz | 45190 | Violet |
| Acid
Red 50 | 45220 | Rot |
| Phenyl-2-oxyfluoron-2-carbonsäure | 45350 | gelb |
| Chemische
oder sonstige Bezeichnung | CIN | Farbe |
| 4,5-Dibromfluorescein | 45370 | Orange |
| 2,4,5,7-Tetrabromfluorescein | 45380 | Rot |
| Solvent
Dye | 45396 | Orange |
| Acid
Red 98 | 45405 | Rot |
| 3',4',5',6'-Tetrachlor-2,4,5,7-tetrabromfluorescein | 45410 | Rot |
| 4,5-Diiodfluorescein | 45425 | Rot |
| 2,4,5,7-Tetraiodfluorescein | 45430 | Rot |
| Chinophthalon | 47000 | Gelb |
| Chinophthalon-disulfosäure | 47005 | Gelb |
| Acid
Violet 50 | 50325 | Violett |
| Acid
Black 2 | 50420 | Schwarz |
| Pigment
Violet 23 | 51319 | Violett |
| 1,2-Dioxyanthrachinon,
Calcium-Sluminiumkomplex | 58000 | Rot |
| 3-Oxypyren-5,8,10-sulfosäure | 59040 | Grün |
| 1-Hydroxy-4-N-phenyl-aminoanthrachinon | 60724 | Violett |
| 1-Hydroxy-4-(4'-methylphenylamino)-anthrachinon | 60725 | Violett |
| Acid
Violet 23 | 60730 | Violett |
| 1,4-Di(4'-methyl-phenylamino)-anthrachinon | 61565 | Grün |
| 1,4-Bis-(o-sulfo-p-toluidino)-anthrachinon | 61570 | Grün |
| Acid
Blue 80 | 61585 | Blau |
| Acid
Blue 62 | 62045 | Blau |
| N,N'-Dihydro-1,2,1',2'-anthrachinonazin | 69800 | Blau |
| Vat
Blue 6; Pigment Blue 64 | 69825 | Blau |
| Vat
Orange 7 | 71105 | orange |
| Indigo | 73000 | Blau |
| Indigo-disulfosäure | 73015 | Blau |
| 4,4'-Dimethyl-6,6'-dichlorthioindigo | 73360 | Rot |
| 5,5'Dichlor-7,7'-dimethylthioindigo | 73385 | violett |
| Quinacridone
Violet 19 | 73900 | violett |
| Pigment
Red 122 | 73915 | Rot |
| Chemische
oder sonstige Bezeichnung | CIN | Farbe |
| Pigment
Blue 16 | 74100 | blau |
| Phthalocyanine | 74160 | blau |
| Direct
Blue 86 | 74180 | blau |
| Chlorierte
Phthalocyanine | 74260 | grün |
| Natural
Yellow 6, 19; Natural Red 1 | 75100 | gelb |
| Bixin,
Nor-Bixin | 75120 | orange |
| Lycopin | 75125 | gelb |
| trans-alpha-,
bet- bzw. gamma-Carotin | 75130 | orange |
| Keto-
und/oder Hydroxylderivate des Carotins | 75135 | gelb |
| Guanin
oder Perlglanzmittel | 75170 | weiß |
| 1,7-Bis-(4-hydroxy-3-methoxyphenyl)1,6-heptadien-3,5-dion | 75300 | gelb |
| Komplexsalz
(Na, Al, Ca) der Karminsäure | 75470 | Rot |
| Chlorophyll
a und b; Kupferverbindungen der Chlorophylle und Chlorophylline | 75810 | grün |
| Aluminium | 77000 | weiß |
| Tonerdehydrat | 77002 | weiß |
| Wasserhaltige
Aluminiumsilikate | 77004 | weiß |
| Ultramarin | 77007 | blau |
| Pigment
Red 101 und 102 | 77015 | Rot |
| Bariumsulfat | 77120 | weiß |
| Bismutoxychlorid
und seine Gemische mit Glimmer | 77163 | weiß |
| Calciumcarbonat | 77220 | weiß |
| Calciumsulfat | 77231 | weiß |
| Kohlenstoff | 77266 | schwarz |
| Pigment
Black 9 | 77267 | schwarz |
| Carbo
medicinalis vegetabilis | 77268
:1 | schwarz |
| Chromoxid | 77288 | grün |
| Chromoxid,
wasserhaltig | 77278 | grün |
| Pigment
Blue 28, Pigment Green 14 | 77346 | grün |
| Chemische
oder sonstige Bezeichnung | CIN | Farbe |
| Pigment
Metal 2 | 77400 | braun |
| Gold | 77480 | braun |
| Eisenoxide
und -hydoxide | 77489 | orange |
| Eisenoxid | 77491 | rot |
| Eisenoxidhydrat | 77492 | gelb |
| Eisenoxid | 77499 | schwarz |
| Mischungen
aus Eisen(II)- und Eisen(III)-hexacyahoferrat | 77510 | blau |
| Pigment
White 18 | 77713 | weiß |
| Mangananimoniumdiphosphat | 77742 | violett |
| Manganphosphat;
Mn3(PO4)2·7 H2O | 77745 | rot |
| Silber | 77820 | weiß |
| Titandioxid
und seine Gemische mit Glimmer | 77891 | weiß |
| Zinkoxid | 77947 | weiß |
| 6,7-Dimethyl-9-(1'-D-ribityl)-isoalloxazin,
Lactoflavin | | gelb |
| Zuckerkulör | | braun |
| Capsanthin,
Capsorubin | | orange |
| Betanin | | rot |
| Benzopyryliumsalzem,
Anthocyane | | rot |
| Aluminium-,
Zink-, Magnesium- und Calciumstearat | | weiß |
| Bromthymolblau | | blau |
-
Bevorzugt
sind insbesondere die im folgenden aufgelisteten Arten von Perlglanzpigmenten:
- 1. natürliche Perlglanzpigmente, wie
z. B.
– "Fischsilber" (Guanin/Hypoxanthin-Mischkristalle
aus Fischschuppen) und
– "Perlmutt" (vermahlene Muschelschalen)
- 2. monokristalline Perlglanzpigmente wie z. B. Bismuthoxychlorid
(BiOCl)
- 3. Schicht-Substrat Pigmente: z. B. Glimmer/Metalloxid
-
Basis
für Perlglanzpigmente sind beispielsweise pulverförmige
Pigmente oder Ricinusöldispersionen von Bismutoxychlorid
und/oder Titandioxid sowie Bismutoxychlorid und/oder Titandioxid
auf Glimmer. Insbesondere vorteilhaft ist z. B. das unter der CIN
77163 aufgelistete Glanzpigment.
-
Vorteilhaft
sind ferner beispielsweise die folgenden Perlglanzpigmentarten auf
Basis von Glimmer/Metalloxid:
| Gruppe | elegung/Schichtdicke | Farbe |
| Silberweiße
Perlglanzpigmente | TiO2: 40–60 nm | silber |
| Interferenzpigmente | TiO2: 60–80 nm | gelb |
| | TiO2: 80–100 nm | rot |
| | TiO2: 100–140 nm | blau |
| | TiO2: 120–160 nm | grün |
| Farbglanzpigmente | Fe2O3 | bronze |
| | Fe2O3 | kupfer |
| | Fe2O3 | rot |
| | Fe2O3 | rotviolett |
| | Fe2O3 | rotgrün |
| | Fe2O3 | schwarz |
| Kombinationspigmente | TiO2/Fe2O3 | goldtöne |
| | TiO2/Cr2O3 | grün |
| | TiO2/Berliner Blau | tiefblau |
-
Besonders
bevorzugt sind z. B. die von der Firma Merck unter den Handelsnamen
Timiron®, Colorona®,
Dichrona®, Xirona® oder
Ronastar® erhältlichen
Perlglanzpigmente.
-
Die
Liste der genannten Perlglanzpigmente soll selbstverständlich
nicht limitierend sein. Im Sinne der vorliegenden Erfindung vorteilhafte
Perlglanzpigmente sind auf zahlreichen, an sich bekannten Wegen
erhältlich. Beispielsweise lassen sich auch andere Substrate
außer Glimmer mit weiteren Metalloxiden beschichten, wie
z. B.
-
Silica
und dergleichen mehr. Vorteilhaft sind Z. B. mit TiO2 und
Fe2O3 beschichtete
SiO2-Partikel ("Ronaspheren"), die von der
Firma Merck vertrieben werden und sich besonders für die
optische Reduktion feiner Fältchen eignen.
-
Es
kann darüber hinaus von Vorteil sein, gänzlich
auf ein Substrat wie Glimmer zu verzichten. Besonders bevorzugt
sind Perlglanzpigmente, welche unter der Verwendung von SiO2 hergestellt werden. Solche Pigmente, die
auch zusätzlich gonichromatische Effekte haben können,
sind z. B. unter dem Handelsnamen Sicopearl Fantastico bei der Firma
BASF erhältlich.
-
Weiterhin
vorteilhaft können Pigmente der Firma Engelhard/Mearl auf
Basis von Calcium Natrium Borosilikat, die mit Titandioxid beschichtet
sind, eingesetzt werden. Diese sind unter dem Namen Reflecks® erhältlich. Sie weisen
durch ihre Partikelgröße von 40–80 μm
zusätzlich zu der Farbe einen Glitzereffekt auf.
-
Besonders
vorteilhaft sind ferner auch Effektpigmente, welche unter der Handelsbezeichnung
Metasomes® Standard/Glitter in
verschiedenen Farben (yellow, red, green, blue) von der Firma Flora
Tech erhältlich sind. Die Glitterpartikel liegen hierbei
in Gemischen mit verschiedenen Hilfs- und Farbstoffen (wie beispielsweise
den Farbstoffen mit den Colour Index (Cl) Nummern 19140, 77007,
77289, 77491) vor.
-
Die
erfindungsgemäße Zubereitung oder Mischung kann
darüber hinaus bevorzugt auch weitere Aktivsubstanzen enthalten,
wie zum Beispiel Repellentien, insbesondere Mittel zur Insektenabwehr,
UV-Filter, Aryloxime und Parabene.
-
Die
meisten Repellent-Wirkstoffe gehören den Stoffklassen der
Amide, Alkohole, Ester und Ether an. Repellentien sollen dabei üblicherweise
die folgenden Bedingungen erfüllen: Sie dürfen
nicht zu schnell verdunsten und nicht in die Haut eindringen. Sie
dürfen auf die Haut weder primär irritierend noch
sensibilisierend wirken und sollen außerdem nicht toxisch
sein. Ihre Wirksamkeit muss auch unter Einwirkung von Hautflüssigkeit
und/oder UV Strahlung erhalten bleiben.
-
Bevorzugte
Repellentien sind ausgewählt aus N,N-Diethyl-3-methylbenzamid,
3-(Acetyl-butyl-amino)-propionsäure Ethylester, Dimethyiphthalat,
Butopyronoxyl, 2,3,4,5-bis-(2-Butylen)-tetrahydro-2-furaldehyd,
N,N-Caprylsäurediethylamid, N,N-Diethylbenzamid, o-Chlor-N,N-dethylbenzamid,
N-(2-Ethylhexyl)-8,9,10-trinorborn-5-en-2,3-dicarboximid, Dimethyicarbat,
Di-n-propylisocinchomeronat, (R)-p-Mentha-1,8-diol, 2-Ethylhexan-1,3-diol,
N-Octyl-bi-cyclohepetendiecarboximid, Piperonyl-butoxid, 1-(2-Methylpropyloxycarbonyl)-2-(hydroxyethyl)piperidin
(Bayrepel®; Fa. Bayer) oder Mischungen
davon, wobei es insbesondere bevorzugt ausgewählt ist aus
N,N-Diethyl-3-methylbenzamid, 3-(Acetyl-butyl amino)-propionsäure-ethylester,
1-(2-Methylpropyloxycarbonyl)-2-(hydroxyethyl)piperidin oder Mischungen
davon.
-
Parabene
sind 4-Hydroxybenzoesäureester, die in freier Form oder
als Natrium-Salze zur Konservierung von Zubereitungen im Bereich
der Nahrungsmittel, Kosmetik und Arzneimittel verwendet werden.
Die Wirkung der Ester ist direkt proportional zur Kettenlänge
des Alkyl-Restes, umgekehrt nimmt jedoch die Löslichkeit mit
steigender Kettenlänge ab. Als nicht dissoziierende Verbindungen
sind die Ester weitgehend pH-Wert-unabhängig und wirken
in einem pH-Bereich von 3,0–8,0. Der antimikrobielle Wirkmechanismus
beruht auf einer Schädigung der Mikrobenmembranen durch
die Oberflächenaktivität der PHB-Ester sowie auf
der Eiweiß-Denaturierung. Daneben treten Interaktionen
mit Coenzymen auf. Die Wirkung richtet sich gegen Pilze, Hefen und
Bakterien. Die als Konservierungsmittel wichtigsten Parabene sind
4-Hydroxybenzoesäuremethylester, 4-Hydroxybenzoesäureethylester,
4-Hydroxybenzoesäurepropylester, 4-Hydroxybenzoesäurebutylester.
-
Unter
den Aryloximen wird vorzugsweise 2-Hydroxy-5-methyllaurophenonoxim,
welches auch als HMLO, LPO oder F5 bezeichnet wird, eingesetzt.
Seine Eignung zum Einsatz in kosmetischen Mitteln ist beispielsweise
aus der Deutschen Offenlegungsschrift
DE 41 16 123 bekannt. Zubereitungen, die 2-Hydroxy-5-methyllaurophenonoxim
enthalten, sind demnach zur Behandlung von Hauterkrankungen, die
mit Entzündungen einhergehen, geeignet. Es ist bekannt,
dass derartige Zubereitungen z. B. zur Therapie der Psioriasis,
unterschiedlicher Ekzemformen, irritativer und toxischer Dermatitis,
UV-Dermatitis sowie weiterer allergischer und/oder entzündlicher
Erkrankungen der Haut und der Hautanhangsgebilde verwendet werden
können. Erfindungsgemäße Zubereitungen,
die neben den genannten Verbindung(en) zusätzlich ein Aryloxim,
vorzugsweise 2-Hydroxy-5-methyllaurophenonoxim, enthalten, zeigen überraschende
antiinflammatorische Eignung. Dabei enthalten die Zubereitungen
vorzugsweise 0,01 bis 10 Gew.-% des Aryloxims, wobei es insbesondere bevorzugt
ist, wenn die Zubereitung 0,05 bis 5 Gew-% Aryloxim enthält.
-
Die
schützende Wirkung von Zubereitungen gegen oxidativen Stress
bzw. gegen die Einwirkung von Radikalen kann verbessert werden,
wenn die Zubereitungen ein oder mehrere Antioxidantien enthalten,
wobei es dem Fachmann keinerlei Schwierigkeiten bereitet geeignet
schnell oder zeitverzögert wirkende Antioxidantien auszuwählen.
-
In
einer bevorzugten Ausführungsform handelt es sich daher
bei der Zubereitung um eine Zubereitung zum Schutz von Körperzellen
gegen oxidativen Stress, insbesondere zur Verringerung der Hautalterung,
dadurch gekennzeichnet, dass sie neben den anderen Inhaltsstoffen
ein oder mehrere Antioxidantien enthält.
-
Es
gibt viele aus der Fachliteratur bekannte und bewährte
Substanzen, die als Antioxidantien verwendet werden können,
z. B. Aminosäuren (z. B. Glycin, Histidin, Tyrosin, Tryptophan)
und deren Derivate, Imidazole, (z. B. Urocaninsäure) und
deren Derivate, Peptide wie D,L-Carnosin, D-Carnosin, L-Carnosin
und deren Derivate (z. B. Anserin), Carotinoide, Carotine (z. B. α-Carotin, β-Carotin,
Lycopin) und deren Derivate, Chlorogensäure und deren Derivate,
Liponsäure und deren Derivate (z. B. Dihydroliponsäure),
Aurothioglucose, Propylthiouracil und andere Thiole (z. B. Thioredoxin,
Glutathion, Cystein, Cystin, Cystamin und deren Glycosyl-, N-Acetyl-,
Methyl-, Ethyl-, Propyl-, Amyl-, Butyl- und Lauryl-, Palmitoyl-,
Oleyl-, γ-Linoleyl, Cholesteryl- und Glycerylester) sowie
deren Salze, Dilaurylthiodipropionat, Distearylthiodipropionat,
Thiodipropionsäure und deren Derivate (Ester, Ether, Peptide,
Lipide, Nukleotide, Nukleoside und Salze) sowie Sulfoximinverbindungen
(z. B. Buthioninsulfoximine, Homocysteinsulfoximin, Buthioninsulfone,
Penta-, Hexa-, Heptathioninsulfoximin) in sehr geringen verträglichen
Dosierungen (z. B. pmol bis μmol/kg), ferner (Metall-)Chelatoren,
(z. B. α-Hydroxyfettsäuren, Palmitinsäure,
Phytinsäure, Lactoferrin), α-Hydroxysäuren
(z. B. Citronensäure, Milchsäure, Äpfelsäure),
Huminsäure, Gallensäure, Gallenextrakte, Bilirubin,
Biliverdin, EDTA, EGTA und deren Derivate, ungesättigte
Fettsäuren und deren Derivate, Vitamin C und Derivate (z.
B. Ascorbylpalmitat, Magnesium-Ascorbylphosphat, Ascorbylacetat),
Tocopherole und Derivate (z. B. Vitamin-E-acetat), Vitamin A und
Derivate (z. B. Vitamin-A-palmitat) sowie Koniferylbenzoat des Benzoeharzes,
Rutinsäure und deren Derivate, α-Glycosylrutin,
Ferulasäure, Furfurylidenglucitol, Carnosin, Butylhydroxytoluol,
Butylhydroxyanisol, Nordohydroguajaretsäure, Trihydroxybutyrophenon,
Quercitin, Harnsäure und deren Derivate, Mannose und deren
Derivate, Zink und dessen Derivate (z. B. ZnO, ZnSO4),
Selen und dessen Derivate (z. B. Selenmethionin), Stilbene und deren
Derivate (z. B. Stilbenoxid, trans-Stilbenoxid).
-
Geeignete
Antioxidantien sind auch Verbindungen der allgemeinen Formeln A
oder B
worin
R
1 aus der Gruppe -C(O)CH
3,
-CO
2R
3, -C(O)NH
2 und -C(O)N(R
4)
2 ausgewählt werden kann,
X
O oder NH,
R
2 lineares oder verzweigtes
Alkyl mit 1 bis 30 C-Atomen,
R
3 lineares
oder verzweigtes Alkyl mit 1 bis 20 C-Atomen,
R
4 jeweils
ungabhängig voneinander H oder lineares oder verzweigtes
Alkyl mit 1 bis 8 C-Atomen,
R
5 lineares
oder verzweigtes Alkyl mit 1 bis 8 C-Atomen oder lineares oder verzweigtes
Alkoxy mit 1 bis 8 C-Atomen und
R
6 lineares
oder verzweigtes Alkyl mit 1 bis 8 C-Atomen bedeutet, vorzugsweise
Derivate der 2-(4-Hydroxy-3,5-dimethoxybenzyliden)-malonsäure
und/oder 2-(4-Hydroxy-3,5-dimethoxybenzyl)-malonsäure,
besonders bevorzugt 2-(4-Hydroxy-3,5-dimethoxybenzyliden)-malonsäure-bis-(2-ethylhexyl)ester
(z. B. Oxynex
® ST Liquid) und/oder
2-(4-Hydroxy-3,5-dimethoxybenzy)-malonsäure-bis-(2-ethylhexyl)ester
(z. B. RonaCare
® AP).
-
Mischungen
von Antioxidantien sind ebenfalls zur Verwendung in den erfindungsgemäßen
kosmetischen Zubereitungen geeignet. Bekannte und käufliche
Mischungen sind beispielsweise Mischungen enthaltend als aktive
Inhaltsstoffe Lecithin, L-(+)-Ascorbylpalmitat und Zitronensäure
(z. B. (z. B. Oxynex® AP), natürliche
Tocopherole, L-(+)-Ascorbylpalmitat, L-(+)-Ascorbinsäure
und Zitronensäure (z. B. Oxynex® K
LIQUID), Tocopherolextrakte aus natürlichen Quellen, L-(+)-Ascorbylpalmitat,
L-(+)-Ascorbinsäure und Zitronensäure (z. B. Oxynex® L LIQUID), DL-α-Tocopherol,
L-(+)-Ascorbylpalmitat, Zitronensäure und Lecithin (z.
B. Oxynex® LM) oder Butylhydroxytoluol
(BHT), L-(+)-Ascorbylpalmitat und Zitronensäure (z. B.
Oxynex® 2004). Derartige Antioxidantien
werden mit den erfindungsgemäßen Verbindungen
in solchen Zusammensetzungen üblicherweise in Gewichtsprozentverhältnissen
im Bereich von 1000:1 bis 1:1000, bevorzugt in Gewichtsprozentverhältnissen
von 100:1 bis 1:100 eingesetzt.
-
Geeignete
Antioxidantien sind ferner Verbindungen der Formel (C)
wobei
R
1 bis
R
10 gleich oder verschieden sein können
und ausgewählt sind aus
- – H
- – OR11
- – geradkettigen oder verzweigten C1-
bis C20-Alkylgruppen,
- – geradkettigen oder verzweigten C3-
bis C20-Alkenylgruppen,
- – geradkettigen oder verzweigten C1 bis
C20-Hydroxyalkylgruppen, wobei die Hydroxygruppe
an ein primäres oder sekundäres Kohlenstoffatom
der Kette gebunden sein kann und weiter die Alkylkette auch durch Sauerstoff
unterbrochen sein kann, und/oder
- – C3- bis C10-Cycloalkylgruppen
und/oder C3- bis C12-Cycloalkenylgruppen,
wobei die Ringe jeweils auch durch -(CH2)-Gruppen
mit n = 1 bis 3 überbrückt sein können,
- – wobei alle OR11 unabhängig
voneinander stehen für
- – OH
- – geradkettige oder verzweigte C1-
bis C20-Alkyloxygruppen,
- – geradkettigen oder verzweigten C3-
bis C20-Alkenyloxygruppen,
- – geradkettigen oder verzweigten C1-
bis C20-Hydroxyalkoxygruppen, wobei die
Hydroxygruppe(n) an ein primäre oder sekundäre
Kohlenstoffatome der Kette gebunden sein können und weiter
die Alkylkette auch durch Sauerstoff unterbrochen sein kann, und/oder
- – C3- bis C10-Cycloalkyloxygruppen
und/oder C3- bis C12-Cycloalkenyloxygruppen,
wobei die Ringe jeweils auch durch -(CH2)n-Gruppen mit n = 1 bis 3 überbrückt
sein können und/oder,
- – Mono- und/oder Oligoglycosylreste,
mit der Maßgabe,
dass mindestens 4 Reste aus R1 bis R7 stehen für OH und dass im Molekül
mindestens 2 Paare benachbarter Gruppen -OH vorliegen,
- – oder R2, R5 und
R6 für OH und die Reste R1, R3, R4 und
R7-10 für H stehen, wie sie in
der Deutschen Patentanmeldung DE-A-102 44 282 beschrieben sind.
-
Die
einzusetzenden Zubereitungen oder Mischungen können als
weitere Inhaltsstoffe Vitamine enthalten. Bevorzugt sind Vitamine
und Vitamin-Derivate ausgewählt aus Vitamin A, Vitamin-A-Propionat,
Vitamin-A-Palmitat, Vitamin-A-Acetat, Retinol, Vitamin B, Thiaminchloridhydrochlorid
(Vitamin B1), Riboflavin (Vitamin B2), Nicotinsäureamid, Vitamin C
(Ascorbinsäure), Vitamin D, Ergocalciferol (Vitamin D2), Vitamin E, DL-α-Tocopherol,
Tocopherol-E-Acetat, Tocopherolhydrogensuccinat, Vitamin K1, Esculin (Vitamin P-Wirkstoff), Thiamin
(Vitamin B1), Nicotinsäure (Niacin),
Pyridoxin, Pyridoxal, Pyridoxamin, (Vitamin B6),
Panthothensäure, Biotin, Polsäure und Cobalamin
(Vitamin B12), insbesondere bevorzugt Vitamin-A-Palmitat,
Vitamin C und dessen Derivate, DL-α-Tocopherol, Tocopherol-E-Acetat,
Nicotinsäure, Pantothensäure und Biotin. Vitamine
werden mit den flavonoidhaltigen Vormischungen oder Zubereitungen üblicherweise
bei kosmetischer Anwendung in Bereichen von 0,01 bis 5,0 Gew.-%,
bezogen auf das Gesamtgewicht, zugesetzt. Ernährungsphysiologische
Anwendungen orientieren sich am jeweiligen empfohlenen Vitaminbedarf.
-
Bevorzugte
Zubereitungen können auch dem Sonnenschutz dienen. Erfindungsgemäße
Zubereitungen oder Mischungen können daher neben α-Aminosäurederivaten
und den schwerlöslichen Substanzen sowie den gegebenenfalls
anderen Inhaltsstoffen auch UV-Filter enthalten.
-
Prinzipiell
kommen alle UV-Filter für eine Kombination mit den erfindungsgemäß einzusetzenden α-Aminosäurederivaten
in Frage. Besonders bevorzugt sind solche UV-Filter, deren physiologische
Unbedenklichkeit bereits nachgewiesen ist.
-
Sowohl
für UVA wie auch UVB-Filter gibt es viele aus der Fachliteratur
bekannte und bewährte Substanzen, z. B.
-
Benzylidenkampferderivate
wie 3-(4''-Methylbenzyliden)-dl-kampfer (z. B. Eusolex® 6300),
3-Benzylidenkampfer (z. B. Mexoryl® SD),
Polymere von N-{(2 und 4)-[(2-oxoborn-3-yliden)methyl]benzyl}-acrylamid
(z. B. Mexoryl® SW) oder N,N,N-Trimethyl-4-(2-oxoborn-3-ylidenmethyi)anilinium
methylsulfat (z. B. Mexoryl® SK).
-
Benzoyl-
oder Dibenzoylmethane wie 1-(4-tert-Butylphenyl)-3-(4-methoxyphenyl)-propan-1,3-dion
(z. B. Eusolex® 9020) oder 4-Isopropyldibenzoylmethan
(z. B. Eusolex® 8020),
Benzophenone
wie 2-Hydroxy-4-methoxybenzophenon (z. B. Eusolex® 4360)
oder das Natriumsalz der 2-Hydroxy-4-methoxybenzophenon-5-sulfonsäure.
-
Methoxyzimtsäureester
wie Methoxyzimtsäureoctylester (z. B. Eusolex® 2292),
4-Methoxyzimtsäureisopentylester, z. B. als Gemisch der
Isomere (z. B. Neo Heliopan® E
1000),
Salicylatderivate wie 2-Ethylhexylsalicylat (z. B. Eusolex® OS), 4-Isopropylbenzylsalicylat
(z. B. Megasol®) oder 3,3,5-Trimethylcyclohexylsalicylat
(z. B. Eusolex® HMS).
-
Kalium-,
Natrium und Triethanolaminsalze der Phenylbenzimidazolsulfonsäuren,
wie 2-Phenylbenzimidazol-5-sulfonsäure, 2,2-(1,4-Phenylen)-bisbenzimidazol-4,6-disulfonsäure
bzw. deren Salze (z. B. Neoheliopan® AP)
und
weitere Substanzen wie
- – 2-Cyano-3,3-diphenylacrylsäure-2-ethylhexylester
(z. B. Eusolex® OCR),
- – 3,3'-(1,4-Phenylendimethylen)-bis-(7,7-dimethyl-2-oxobicyclo-[2.2.1]hept-1-ylmethansulfonsäure
sowie ihre Salze (z. B. Mexoryl® SX)
und
- – 2,4,6-Trianilino-(p-carbo-2''-ethylhexyl-1''-oxi)-1,3,5-triazin
(z. B. Uvinul® T 150)
- – 2-(4-Diethylamino-2-hydroxy-benzoyl)-benzoesäure
hexylester (z. B. Uvinul® UVA Plus,
Fa. BASF).
-
Die
in der Liste aufgeführten Verbindungen sind nur als Beispiele
aufzufassen. Selbstverständlich können auch andere
UV-Filter verwendet werden.
-
Weitere
geeignete organische UV-Filter sind z. B.
- – 2-(2H-Benzotriazol-2-yl)-4-methyl-6-(2-methyl-3-(1,3,3,3-tetramethyl-1-(trimethylsilyloxy)disiloxanyi)propyl)phenol
(z. B. Silatrizole®, Drometrizole,
Trisiloxane, Mexoryl® XL),
- – 4,4''-[(6-[4-((1,1-Dimethylethyl)aminocarbonyl)phenylamino]-1,3,5-triazin-2,4-diyl)diimino]bis(benzoesäure-2-ethylhexylester)
(z. B. Uvasorb® HEB),
- – α-(Trimethylsilyl)-ω-[trimethylsilyl)oxy]poly[oxy(dimethyl
[und ca. 6% methyl[2-[p-[2,2-bis(ethoxycarbonyl]vinyl]phenoxy]-1-methylenethyl]
und ca. 1,5% methyl[3-[p-[2,2-bis(ethoxycarbonyl)vinyl)phenoxy)-propenyl)
und 0,1 bis 0,4% (methylhydrogen]silylen]] (n ≈ 60) (CAS-Nr.
207 574-74-1)
- – 2,2''-Methylen-bis-(6-(2H-benzotriazol-2-yl)-4-(1,1,3,3-tetramethylbutyl)phenol)
(CAS-Nr. 103 597-45-1)
- – 2,2''-(1,4-Phenylen)bis-(1H-benzimidazol-4,6-disulfonsäure,
Mononatriumsalz) (CAS-Nr. 180 898-37-7) und
- – 2,4-bis-{[4-(2-Ethyl-hexyloxy)-2-hydroxyl]-phenyl}-6-(4-methoxyphenyl)-1,3,5-triazin
(CAS-Nr. 103 597-45-, 187 393-00-6).
- – 4,4''-[(6-[4-((1,1-Dimethylethyl)aminocarbonyl)phenylamino]-1,3,5-triazin-2,4-diyl)diimino]bis(benzoesäure-2-ethylhexylester)
(z. B. Uvasorb® HEB),
Weitere
geeignete UV-Filter sind auch Methoxyflavone ensprechend der Deutschen
Patentanmeldung DE-A-10232595 .
-
Organische
UV-Filter werden in der Regel in einer Menge von 0,5 bis 20 Gewichtsprozent,
vorzugsweise 1–15 Gew.-%, in Formulierungen eingearbeitet.
-
Um
einen optimierten UV-Schutz zu gewährleisten ist es weiter
bevorzugt, wenn Zubereitungen mit Lichtschutzeigenschaften auch
anorganische UV-Filter enthalten. Als anorganische UV-Filter sind
solche aus der Gruppe der Titandioxide wie z. B. gecoatetes Titandioxid
(z. B. Eusolex® T-2000, Eusolex® T-AQUA, Eusolex® T-AVO),
Zinkoxide (z. B. Sachtotec®), Eisenoxide
oder auch Ceroxide denkbar. Diese anorganischen UV-Filter werden
in der Regel in einer Menge von 0,5 bis 20 Gewichtsprozent, vorzugsweise
2–10 Gew.-%, in kosmetische Zubereitungen eingearbeitet.
-
Bevorzugte
Verbindungen mit UV-filternden Eigenschaften sind 3-(4''-Methylbenzyliden)-dl-kampfer, 1-(4-tert-Butylphenyl)-3-(4-methoxy-phenyl)-propan-1,3-dion,
4-Isopropyldibenzoylmethan, 2-Hydroxy-4-methoxy-benzophenon, Methoxyzimtsäureoctylester,
3,3,5-Trimethyl-cyclo-hexyl-sali-cylat, 4-(Dimethylamino)benzoesäure-2-ethyl-hexylester,
2-Cyano-3,3-di-phenylacrylsäure-2-ethylhexylester, 2-Phenyl-benzimidazol-5-sulfon-säure
sowie ihre Kalium-, Natrium- und Triethanol-aminsalze.
-
Durch
Kombination von einer oder mehrerer der genannten Verbindungen mit
UV-Filterwirkung kann die Schutzwirkung gegen schädliche
Einwirkungen der UV-Strahlung optimiert werden.
-
Alle
genannten UV-Filter können auch in verkapselter Form eingesetzt
werden. Insbesondere ist es von Vorteil organische UV-Filter in
verkapselter Form einzusetzen. Im Einzelnen ergeben sich die folgende
Vorteile:
- – Die Hydrophilie der Kapselwand
kann unabhängig von der Löslichkeit des UV-Filters
eingestellt werden. So können beispielsweise auch hydrophobe
UV-Filter in rein wässrige Zubereitungen eingearbeitet
werden. Zudem wird der häufig als unangenehm empfundene ölige
Eindruck beim Auftragen der hydrophobe UV-Filter enthaltenden Zubereitung
unterbunden.
- – Bestimmte UV-Filter, insbesondere Dibenzoylmethanderivate,
zeigen in kosmetischen Zubereitungen nur eine verminderte Photostabilität.
Durch Verkapselung dieser Filter oder von Verbindungen, die die
Photostabilität dieser Filter beeinträchtigen,
wie beispielsweise Zimtsäurederivate, kann die Photostabilität
der gesamten Zubereitung erhöht werden.
- – In der Literatur wird immer wieder die Hautpenetration
durch organische UV-Filter und das damit verbundene Reizpotential
beim direkten Auftragen auf die menschliche Haut diskutiert. Durch
die hier vorgeschlagene Verkapselung der entsprechenden Substanzen
wird dieser Effekt unterbunden.
- – Allgemein können durch Verkapselung einzelner
UV-Filter oder anderer Inhaltstoffe Zubereitungsprobleme, die durch
Wechselwirkung einzelner Zubereitungsbestandteile untereinander
entstehen, wie Kristallisationsvorgänge, Ausfällungen
und Agglomeratbildung vermieden werden, da die Wechselwirkung unterbunden
wird.
-
Daher
ist es bevorzugt, wenn ein oder mehrere der oben genannten UV-Filter
in verkapselter Form vorliegen. Vorteilhaft ist es dabei, wenn die
Kapseln so klein sind, dass sie mit dem bloßen Auge nicht
beobachtet werden können. Zur Erzielung der o. g. Effekte
ist es weiterhin erforderlich, dass die Kapseln hinreichend stabil sind
und den verkapselten Wirkstoff (UV-Filter) nicht oder nur in geringem
Umfang an die Umgebung abgeben.
-
Geeignete
Kapseln können Wände aus anorganischen oder organischen
Polymeren aufweisen. Beispielsweise wird in
US 6,242,099 B1 die Herstellung
geeigneter Kapseln mit Wänden aus Chitin, Chitin-Derivaten
oder polyhydroxylierten Polyaminen beschrieben. Besonders bevorzugt
einzusetzende Kapseln weisen Wände auf, die durch einen
SolGel-Prozess, wie er in den Anmeldungen
WO 00/09652 ,
WO 00/72806 und
WO 00/71084 beschrieben ist, erhalten
werden können. Bevorzugt sind hier wiederum Kapseln, deren
Wände aus Kieselgel (Silicat undefiniertes Silicium-Oxid-hydroxid)
aufgebaut sind. Die Herstellung entsprechender Kapseln ist dem Fachmann
beispielsweise aus den zitierten Patentanmeldungen bekannt, deren
Inhalt ausdrücklich auch zum Gegenstand der vorliegenden
Anmeldung gehört.
-
Dabei
sind die Kapseln in erfindungsgemäß einzusetzenden
Zubereitungen vorzugsweise in solchen Mengen enthalten, die gewährleisten,
dass die verkapselten UV-Filter in den oben angegebenen Gewichtsprozentverhältnissen
in der Zubereitung vorliegen.
-
Die
erfindungsgemäß einzusetzenden Zubereitungen können
darüber hinaus weitere übliche hautschonende oder
hautpflegende Wirkstoffe enthalten. Dies können prinzipiell
alle den Fachmann bekannten Wirkstoffe sein.
-
Besonders
bevorzugte Wirkstoffe, insbesondere für hautpflegende Zubereitungen,
sind beispielsweise auch sogenannte kompatible Solute. Es handelt
sich dabei um Substanzen, die an der Osmoregulation von Pflanzen
oder Mikroorganismen beteiligt sind und aus diesen Organismen isoliert
werden können. Unter den Oberbegriff kompatible Solute
werden dabei auch die in der Deutschen Patentanmeldung
DE-A-10133202 beschriebenen
Osmolyte gefasst. Geeignete Osmolyte sind beispielsweise die Polyole,
Methylamin- Verbindungen und Aminosäuren sowie jeweils
deren Vorstufen. Als Osmolyte werden im Sinne der Deutschen Patentanmeldung
DE-A-10133202 insbesondere
Substanzen aus der Gruppe der Polyole, wie beispielsweise myo-Inositol,
Mannitol oder Sorbitol und/oder einer oder mehrere der nachfolgend
genannten osmolytisch wirksamen Stoffe verstanden: Taurin, Cholin,
Betain, Phosphorylcholin, Glycerophosphorylcholine, Glutamin, Glycin, α-Alanin,
Glutamat, Aspartat, Prolin, und Taurin. Vorstufen dieser Stoffe
sind beispielsweise Glucose, Glucose-Polymere, Phosphatidylcholin,
Phosphatidylinositol, anorganische Phosphate, Proteine, Peptide
und Polyaminsäuren. Vorstufen sind z. B. Verbindungen,
die durch metabolische Schritte in Osmolyte umgewandelt werden.
-
In
den erfindungsgemäßen Zubereitungen oder Mischungen
können kompatible Solute, wie zuvor beschrieben, vorzugsweise
in Mengen bis zu 15 Gew.-% eingesetzt werden.
-
Insbesondere
bevorzugt ist es dabei, wenn die kompatiblen Solute ausgewählt
sind aus Di-myo-inositol-phosphat (DIP), cyclisches 2,3-diphosphoglycerat
(cDPG), 1,1-Diglycerin-Phosphat (DGP), β-Mannosylglycerat
(Firoin), β-Mannosylglyceramid (Firoin-A) oder/und Di-mannosyl-di-inositolphosphat
(DMIP) oder Mischungen davon.
-
Ferner
können die erfindungsgemäßen Zubereitungen
oder Mischungen mindestens einen Selbstbräuner als weiteren
Inhaltsstoff enthalten.
-
Als
vorteilhafte Selbstbräuner können unter anderem
eingesetzt werden:
-
Ferner
ist das 5-Hydroxy-1,4-naphtochinon (Juglon) zu nennen, das aus den
Schalen frischer Walnüsse extrahiert wird
5-Hydroxy-1,4-naphtochinon
(Juglon)
sowie das in den Henna-Blättern vorkommende
2-Hydroxy-1,4-naphtochinon (Lawson).
2-Hydroxy-1,4-naphtochinon
(Lawson)
-
Ganz
besonders bevorzugt ist das 1,3-Dihydroxyaceton (DHA), ein im menschlichen
Körper vorkommender dreiwertiger Zucker und dessen Derivate
1,3-Dihydroxyaceton
(DHA)
-
Die α-Aminosäurederivate
und die schwerlöslichen Substanzen sowie die gegebenenfalls
weiteren Wirkstoffe können in der üblichen Weise,
beispielsweise durch Mischen, in kosmetische oder dermatologische Zubereitungen
eingearbeitet werden.
-
Geeignet
sind Zubereitungen für eine äußerliche
Anwendung, beispielsweise als Creme, Lotion, Gel, oder als Lösung,
die auf die Haut aufgesprüht werden kann. Für
eine innerliche Anwendung sind Darreichungsformeln wie Kapseln,
Dragees, Pulver, Tabletten-Lösungen oder Lösungen
geeignet.
-
Als
Anwendungsform der einzusetzenden Zubereitungen seien z. B. genannt:
Lösungen, Suspensionen, Emulsionen, PIT-Emulsionen, Pasten,
Salben, Gele, Cremes, Lotionen, Puder, Seifen, tensidhaltige Reinigungspräparate, Öle,
Aerosole und Sprays. Bevorzugte Anwendungsformen sind auch Shampoos,
Sonnenbäder und Duschbäder, die auch als sog. „Spray
Tanning, Airbrush Tanning oder Sonnenduschen "aus kommerziellen
Selbstbräunungs-Studios bekannt sind.
-
Bevorzugte
Hilfsstoffe stammen aus der Gruppe der Konservierungsstoffe, Stabilisatoren,
Lösungsvermittler, Färbemittel, Geruchsverbesserer.
-
Salben,
Pasten, Cremes und Gele können die üblichen Trägerstoffe
enthalten, z. B. tierische und pflanzliche Fette, Wachse, Paraffine,
Stärke, Traganth, Cellulosederivate, Polyethylenglykole,
Silicone, Bentonite, Kieselsäure, Talkum und Zinkoxid oder
Gemische dieser Stoffe.
-
Puder
und Sprays können die üblichen Trägerstoffe
enthalten, z. B. Milchzucker, Talkum, Kieselsäure, Aluminiumhydroxid,
Calciumsilikat und Polyamid-Pulver oder Gemische dieser Stoffe.
Sprays können zusätzlich die üblichen
leichtflüchtigen, verflüssigten Treibmittel, z.
B. Chlorfluorkohlenwasserstoffe, Propan/Butan oder Dimethylether,
enthalten. Auch Druckluft ist vorteilhaft zu verwenden.
-
Lösungen
und Emulsionen können die üblichen Trägerstoffe
wie Lösungsmittel, Lösungsvermittler und Emulgatoren,
z. B. Wasser, Ethanol, Isopropanol, Ethylcarbonat, Ethylacetat,
Benzylalkohol, Benzylbenzoat, Propylenglykol, 1,3-Butylglykol, Öle,
insbesondere Baumwollsaatöl, Erdnussöl, Maiskeimöl, Olivenöl,
Rizinusöl und Sesamöl, Glycerinfettsäureester,
Polyethylenglykole und Fettsäureester des Sorbitans oder
Gemische dieser Stoffe enthalten.
-
Suspensionen
können die üblichen Trägerstoffe wie
flüssige Verdünnungsmittel, z. B. Wasser, Ethanol oder
Propylenglykol, Suspendiermittel, z. B. ethoxylierte Isostearylalkohole,
Polyoxyethylensorbitester und Polyoxyethylensorbitanester, mikrokristalline
Cellulose, Aluminiummetahydroxid, Bentonit, Agar-Agar und Traganth
oder Gemische dieser Stoffe enthalten.
-
Seifen
können die üblichen Trägerstoffe wie
Alkalisalze von Fettsäuren, Salze von Fettsäurehalbestern,
Fettsäureeiweißhydrolysaten, Isothionate, Lanolin,
Fettalkohol, Pflanzenöle, Pflanzenextrakte, Glycerin, Zucker
oder Gemische dieser Stoffe enthalten.
-
Tensidhaltige
Reinigungsprodukte können die üblichen Trägerstoffe
wie Salze von Fettalkoholsulfaten, Fettalkoholethersulfaten, Sulfobernsteinsäurehalbestern,
Fettsäureeiweißhydrolysaten, Isothionate, Imidazoliniumderivate,
Methyltaurate, Sarkosinate, Fettsäureamidethersulfate,
Alkylamidobetaine, Fettalkohole, Fettsäureglyceride, Fettsäurediethanolamide,
pflanzliche und synthetische Öle, Lanolinderivate, ethoxylierte
Glycerinfettsäureester oder Gemische dieser Stoffe enthalten.
-
Gesichts-
und Körperöle können die üblichen
Trägerstoffe wie synthetische Öle wie Fettsäureester, Fettalkohole,
Silikonöle, natürliche Öle wie Pflanzenöle
und ölige Pflanzenauszüge, Paraffinöle,
Lanolinöle oder Gemische dieser Stoffe enthalten.
-
Weitere
typische kosmetische Anwendungsformen sind auch Lippenstifte, Lippenpflegestifte,
Puder-, Emulsions- und Wachs-Make up sowie Sonnenschutz-, Prä-Sun-
und After-Sun-Präparate.
-
Zu
den bevorzugten Zubereitungsformen gehören insbesondere
auch Emulsionen.
-
Emulsionen
sind vorteilhaft und enthalten z. B. die genannten Fette, Öle,
Wachse und anderen Fettkörper, sowie Wasser und einen Emulgator,
wie er üblicherweise für einen solchen Typ der
Zubereitung verwendet wird.
-
Die
Lipidphase kann vorteilhaft gewählt werden aus folgender
Substanzgruppe:
- – Mineralöle,
Mineralwachse
- – Öle, wie Triglyceride der Caprin- oder der
Caprylsäure, ferner natürliche Öle wie
z. B. Rizinusöl;
- – Fette, Wachse und andere natürliche und
synthetische Fettkörper, vorzugsweise Ester von Fettsäuren
mit Alkoholen niedriger C-Zahl, z. B. mit Isopropanol, Propylenglykol
oder Glycerin, oder Ester von Fettalkoholen mit Alkansäuren
niedriger C-Zahl oder mit Fettsäuren;
- – Silikonöle wie Dimethylpolysiloxane, Diethylpolysiloxane,
Diphenylpolysiloxane sowie Mischformen daraus.
-
Die Ölphase
der Emulsionen, Oleogele bzw. Hydrodispersionen oder Lipodispersionen
im Sinne der vorliegenden Erfindung wird vorteilhaft gewählt
aus der Gruppe der Ester aus gesättigtem und/oder ungesättigten,
verzweigten und/oder unverzweigten Alkancarbonsäuren einer
Kettenlänge von 3 bis 30 C-Atomen und gesättigten
und/oder ungesättigten, verzweigten und/oder unverzweigten
Alkoholen einer Kettenlänge von 3 bis 30 C-Atomen, aus
der Gruppe der Ester aus aromatischen Carbonsäure und gesättigten
und/oder ungesättigten, verzweigten und/oder unverzweigten
Alkoholen einer Kettenlänge von 3 bis 30 C-Atomen. Solche Esteröle
können dann vorteilhaft gewählt werden aus der
Gruppe Isopropylmyristat, Isopropylpalmitat, Isopropylstearat, Isopropyloleat,
n-Butylstearat, n-Hexyllaurat, n-Decyloleat, Isooctylstearat, Isononylstearat,
Isononylisononanoat, 2-Ethylhexylpalmitat, 2-Ethylhexyllaurat, 2-Hexaldecylstearat,
2-Octyldodecylpalmitat, Oleyloleat, Oleylerucat, Erucyloleat, Erucylerucat
sowie synthetische, halbsynthetische und natürliche Gemische
solcher Ester, z. B. Jojobaöl.
-
Ferner
kann die Ölphase vorteilhaft gewählt werden aus
der Gruppe der verzweigten und unverzweigten Kohlenwasserstoffe
und -wachse, der Silikonöle, der Dialkylether, der Gruppe
der gesättigten oder ungesättigten, verzweigten
oder unverzweigten Alkohole, sowie der Fettsäuretriglyceride,
namentlich der Triglycerinester gesättigter und/oder ungesättigter,
verzweigter und/oder unverzweigter Alkancarbonsäuren einer
Kettenlänge von 8 bis 24, insbesondere 12-18 C-Atomen.
Die Fettsäuretriglyceride können beispielsweise
vorteilhaft gewählt werden aus der Gruppe der synthetischen,
halbsynthetischen und natürlichen Öle, z. B. Olivenöl, Sonnenblumenöl,
Sojaöl, Erdnussöl, Rapsöl, Mandelöl,
Palmöl, Kokosöl, Palmkernöl und dergleichen
mehr.
-
Auch
beliebige Abmischungen solcher Öl- und Wachskomponenten
sind vorteilhaft im Sinne der vorliegenden Erfindung einzusetzen.
Es kann auch gegebenenfalls vorteilhaft sein, Wachse, beispielsweise
Cetylpalmitat, als alleinige Lipidkomponente der Ölphase
einzusetzen.
-
Die
wässrige Phase der einzusetzenden Zubereitungen enthält
gegebenenfalls vorteilhaft Alkohole, Diole oder Polyole niedriger
C-Zahl, sowie deren Ether, vorzugsweise Ethanol, Isopropanol, Propylenglykol, Glycerin,
Ethylenglykol, Ethylenglykolmonoethyl- oder -monobutylether, Propylenglykolmonomethyl,
-monoethyl- oder- -monobutylether, Diethylenglykolmonomethyl- oder
-monoethylether und analoge Produkte, ferner Alkohole niedriger
C-Zahl, z. B. Ethanol, Isopropanol, 1,2-Propandiol, Glycerin sowie
insbesondere ein oder mehrere Verdickungsmittel, welches oder welche
vorteilhaft gewählt werden können aus der Gruppe
Siliciumdioxid, Aluminiumsilikate, Polysaccharide bzw. deren Derivate,
z. B. Hyaluronsäure, Xanthangummi, Hydroxypropylmethylcellulose,
besonders vorteilhaft aus der Gruppe der Polyacrylate, bevorzugt
ein Polyacrylat aus der Gruppe der sogenannten Carbopole, beispielsweise
Carbopole der Typen 980, 981, 1382, 2984, 5984, jeweils einzeln
oder in Kombination.
-
Insbesondere
werden Gemische der vorstehend genannten Lösemittel verwendet.
Bei alkoholischen Lösemitteln kann Wasser ein weiterer
Bestandteil sein.
-
Emulsionen
sind vorteilhaft und enthalten z. B. die genannten Fette, Öle,
Wachse und anderen Fettkörper, sowie Wasser und einen Emulgator,
wie er üblicherweise für einen solchen Typ der
Formulierung verwendet wird.
-
In
einer bevorzugten Ausführungsform enthalten die einzusetzenden
Zubereitungen hydrophile Tenside. Die hydrophilen Tenside werden
bevorzugt gewählt aus der Gruppe der Alkylglucoside, der
Acyllactylate, der Betaine sowie der Cocoamphoacetate.
-
Es
ist ebenfalls von Vorteil, natürliche oder synthetische
Roh- und Hilfsstoffe bzw. Gemische einzusetzen, welche sich durch
einen wirksamen Gehalt an den erfindungsgemäß verwendeten
Wirkstoffen auszeichnen, beispielsweise Plantaren® 1200
(Henkel KGaA), Oramix® NS 10 (Seppic).
-
Die
kosmetischen und dermatologischen Zubereitungen können
in verschiedenen Formen vorliegen. So können sie z. B.
eine Lösung, eine wasserfreie Zubereitung, eine Emulsion
oder Mikroemulsion vom Typ Wasser-in-Öl (W/O) oder vom
Typ Öl-in-Wasser (O/W), eine multiple Emulsion, beispielsweise
vom Typ Waser-in-Öl-in-Wasser (W/O/W), ein Gel, einen festen
Stift, eine Salbe oder auch ein Aerosol darstellen. Es ist auch
vorteilhaft, Ectoine in verkapselter Form darzureichen, z. B. in
Kollagenmatrices und anderen üblichen Verkapselungsmaterialien,
z. B. als Celluloseverkapselungen, in Gelatine, Wachsmatrices oder
liposomal verkapselt. Insbesondere Wachsmatrices wie sie in der
DE-A-43 08 282 beschrieben
werden, haben sich als günstig herausgestellt. Bevorzugt
werden Emulsionen. O/W-Emulsinen werden besonders bevorzugt. Emulsionen,
W/O-Emulsionen und O/W-Emulsionen sind in üblicher Weise
erhältlich.
-
Als
Emulgatoren können beispielsweise die bekannten W/O- und
O/W-Emulgatoren verwendet werden. Es ist vorteilhaft, weitere übliche
Co-Emulgatoren in den bevorzugten O/W-Emulsionen zu verwenden.
-
Vorteilhaft
werden als Co-Emulgatoren beispielsweise O/W-Emulgatoren gewählt,
vornehmlich aus der Gruppe der Substanzen mit HLB-Werten von 11–16,
ganz besonders vorteilhaft mit HLB-Werten von 14,5–15,5,
sofern die O/W-Emulgatoren gesättigte Reste R und R' aufweisen.
Weisen die O/W-Emulgatoren ungesättigte Reste R und/oder
R' auf, oder liegen Isoalkylderivate vor, so kann der bevorzugte
HLB-Wert solcher Emulgatoren auch niedriger oder darüber
liegen.
-
Es
ist von Vorteil, die Fettalkoholethoxylate aus der Gruppe der ethoxylierten
Stearylalkhole, Cetylalkohole, Cetylstearylalkohole (Cetearylalkohole)
zu wählen. Insbesondere bevorzugt sind: Polyethylenglycol(13)stearylether
(Steareth-13), Polyethylenglycol(14)stearylether (Steareth-14),
Polyethylenglycol(15)stearylether (Steareth-15), Polyethylenglycol(16)stearylether
(Steareth-16), Polyethylenglycol(17)stearylether (Steareth-17),Polyethylenglycol(18)stearylether
(Steareth-18), Polyethylenglycol(19)stearylether (Steareth-19),
Polyethylenglycol(20)stearylether (Steareth-20), Polyethylenglycol(12)isostearylether
(Isosteareth-12), Polyethylenglycol(13)isostearylether (Isosteareth-13),
Polyethylenglycol(14)isostearylether (Isosteareth-14), Polyethylenglycol(15)isostearylether
(Isosteareth-15), Polyethylenglycol(16)isostearylether (Isosteareth-16),
Polyethylenglycol(17)isostearylether (Isosteareth-17), Polyethylenglycol(18)isostearylether
(Isosteareth-18), Polyethylenglycol(19)isostearylether (Isosteareth-19),
Polyethylenglycol(20) isostearylether (Isosteareth-20), Polyethylenglycol(13)cetylether
(Ceteth-13), Polyethylenglycol(14)cetylether (Ceteth-14), Polyethylenglycol(15)cetylether
(Ceteth-15), Polyethylenglycol(16)cetylether (Ceteth-16), Polyethylenglycol(17)cetylether
(Ceteth-17), Polyethylenglycol(18)cetylether (Ceteth-18), Polyethylenglycol(19)cetylether
(Ceteth-19), Polyethylen-glycol(20)cetylether (Ceteth-20), Polyethylenglycol(13)isocetylether
(Isoceteth-13), Polyethylenglycol(14)isocetylether (Isoceteth-14),
Polyethylenglycol(15)isocetylether (Isoceteth-15), Polyethylenglycol(16)isocetylether
(Isoceteth-16), Polyethylenglycol(17)isocetylether (Isoceteth-17),
Polyethylenglycol(18)isocetylether (Isoceteth-18), Polyethylenglycol(19)isocetylether
(Isoceteth-19), Polyethylenglycol(20)isocetylether (Isaceteth-20),
Polyethylenglycol(12)oleylether (Oleth-12), Polyethylenglycol(13)oleylether
(Oleth-13), Polyethylenglycol(14)oleylether (Oleth-14), Polyethylenglycol(15)oleylether
(Oleth-15), Polyethylenglycol(12)laurylether (Laureth-12), Polyethylenglycol(12)isolaurylether
(Isolaureth-12), Polyethylenglycol(13)cetylstearylether (Ceteareth-13),
Polyethylenglycol(14)cetylstearylether (Ceteareth-14), Polyethylenglycol(15)cetylstearylether
(Ceteareth-15), Polyethylenglycol(16)cetylstearylether (Ceteareth-16),
Polyethylenglycol(17)cetylstearylether (Ceteareth-17), Polyethylenglycol(18)cetyistearylether
(Ceteareth-18), Polyethylenglycol(19)cetylstearylether (Ceteareth-19),
Polyethylenglycol(20)cetylstearylether (Ceteareth-20).
-
Es
ist ferner von Vorteil, die Fettsäureethoxylate ausfolgender
Gruppe zu wählen: Polyethylenglycol(20)stearat, Polyethylenglycol(21)stearat,
Polyethylenglycol(22)stearat, Polyethylenglycol(23)stearat, Polyethylenglycol(24)stearat,
Polyethylenglycol(25)stearat, Polyethylenglycol(12)isostearat, Polyethylenglycol(13)isostearat,
Polyethylenglycol(14)isostearat, Polyethylenglycol(15)isostearat,
Polyethylenglycol(16)isostearat, Polyethylenglycol(17)isostearat,
Polyethylenglycol(18)isostearat, Polyethylenglycol(19)isostearat,
Polyethylenglycol(20)isostearat, Polyethylenglycol(21)isostearat,
Polyethylenglycol(22)isostearat, Polyethylenglycol(23)isostearat,
Polyethylenglycol(24)isostearat, Polyethylenglycol(25)isostearat,
Polyethylenglycol(12)oleat, Polyethylenglycol(13)oleat, Polyethylenglycol(14)oleat,
Polyethylenglycol(15)oleat, Polyethylenglycol(16)oleat, Polyethylenglycol(17)oleat,
Polyethylenglycol(18)oleat, Polyethylenglycol(19)oleat, Polyethylenglycol(20)oleat.
-
Als
ethoxylierte Alkylethercarbonsäure bzw. deren Salz kann
vorteilhaft das Natriumlaureth-11-carboxylat verwendet werden. Als
Alkylethersulfat kann Natrium Laureth1-4sulfat vorteilhaft verwendet
werden. Als ethoxyliertes Cholesterinderivat kann vorteilhaft Polyethylenglycol(30)Cholesterylether
verwendet werden. Auch Polyethylenglycol(25)Sojasterol hat sich
bewährt. Als ethoxylierte Triglyceride können
vorteilhaft die Polyethylenglycol(60) Evening Primrose Glycerides
verwendet werden (Evening Primrose = Nachtkerze).
-
Weiterhin
ist von Vorteil, die Polyethylenglycolglycerinfettsäureester
aus der Gruppe Polyethylenglycol(20)glyceryllaurat, Polyethylenglycol(21)glyceryllaurat,
Polyethylenglycol)(22)glyceryllaurat, Polyethylenglycol(23)glyceryllaurat,
Polyethylenglycol(6)glycerylcaprat/cprinat, Polyethylenglycol(20)glyceryloleat,
Polyethylenglycol)(20)glycerylisostearat, Polyethylenglycol(18)glyceryloleat(cocoat)
zu wählen.
-
Es
ist ebenfalls günstig, die Sorbitanester aus der Gruppe
Polyethylenglycol(20)sorbitanmonolaurat, Polyethylenglycol(20)sorbitanmonostearat,
Polyethylenglycol(20)sorbitanmonoisostearat, Polyethylenglycol(20)sorbitanmonopalmitat,
Polyethylenglycol(20)sorbitanmonooleat zu wählen.
-
Als
fakultative, dennoch erfindungsgemäß gegebenenfalls
vorteilhafte W/O-Emulgatoren können eingesetzt werden:
Fettalkohole
mit 8 bis 30 Kohlenstoffatomen, Monoglycerinester gesättigter
und/oder ungesättigter, verzweigter und/oder unverzweigter
Alkancarbonsäuren einer Kettenlänge von 8 bis
24, insbesondere 12-18 C-Atome, Diglycerinester gesättigter
und/oder ungesättigter, verzweigter und/oder unverzweigter
Alkancarbonsäuren einer Kettenlänge von 8 bis
24, insbesondere 12-18 C-Atomen, Monoglycerinether gesättigter
und/oder ungesättigter, verzweigter und/oder unverzweigter
Alkohole einer Kettenlänge von 8 bis 24, insbesondere 12-18 C-Atomen,
Diglycerinether gesättigter und/oder ungesättigter,
verzweigter und/oder unverzweigter Alkohole einer Kettenlänge
von 8 bis 24, insbesondere 12-18 C-Atomen, Propylenglycolester gesättigter
und/oder ungesättigter, verzweigter und/oder unverzweigter
Alkancarbonsäuren einer Kettenlänge von 8 bis
24, insbesondere 12-18 C-Atomen sowie Sorbitanester gesättigter
und/oder ungesättigter, verzweigter und/oder unverzweigter
Alkancarbonsäuren einer Kettenlänge von 8 bis
24, insbesondere 12-18 C-Atomen.
-
Insbesondere
vorteilhafte W/O-Emulgatoren sind Glycerylmonostearat, Glycerylmonoisostearat,
Glycerylmonomyristat, Glycerylmonooleat, Diglycerylmonostearat,
Diglycerylmonoisostearat, Propylenglycolmonostearat, Propylenglycolmonoisostearat,
Propylenglycolmonocaprylat, Propylengiycolmonolaurat, Sorbitanmonoisostearat,
Sorbitanmonolaurat, Sorbitanmonocaprylat, Sorbitanmonoisooleat,
Saccharosedistearat, Cetylalkohol, Stearylalkohol, Arachidylalkohol,
Behenylalkohol, Isobehenylalkohol, Selachylalkohol, Chimylalkohol,
Polyethylenglycol(2)stearylether (Steareth-2), Glycerylmonolaurat,
Glycerylmonocaprinat, Glycerylmonocaprylat.
-
Erfindungsgemäß bevorzugte
Zubereitungen eignen sich auch zum Schutz menschlicher Haut gegen Alterungsprozesse
sowie vor oxidativem Stress, d. h. gegen Schädigungen durch
Radikale, wie sie z. B. durch Sonneneinstrahlung, Wärme
oder andere Einflüsse erzeugt werden. Dabei liegt sie in
verschiedenen, für diese Anwendung üblicherweise
verwendeten Darreichungsformen vor. So kann sie insbesondere als
Lotion oder Emulsion, wie als Creme oder Milch (O/W, W/O, O/W/O,
W/O/W), in Form ölig-alkoholischer, ölig-wässriger oder
wässrig-alkoholischer Gele bzw. Lösungen, als
feste Stifte vorliegen oder als Aerosol konfektioniert sein.
-
Die
Zubereitung kann kosmetische Adjuvantien enthalten, welche in dieser
Art von Zubereitungen üblicherweise verwendet werden, wie
z. B. Verdickungsmittel, weichmachende Mittel, Befeuchtungsmittel,
grenzflächenaktive Mittel, Emulgatoren, Konservierungsmittel,
Mittel gegen Schaumbildung, Parfums, Wachse, Lanolin, Treibmittel,
Farbstoffe und/oder Pigmente, welche das Mittel selbst oder die
Haut färben, und andere in der Kosmetik gewöhnlich
verwendete Ingredienzien.
-
Man
kann als Dispersions- bzw. Solubilisierungsmittel ein Öl,
Wachs oder sonstigen Fettkörper, einen niedrigen Monoalkohol
oder ein niedriges Polyol oder Mischungen davon verwenden. Zu den
besonders bevorzugten Monoalkoholen oder Polyolen zählen
Ethanol, i-Propanol, Propylenglykol, Glycerin und Sorbit.
-
Eine
bevorzugte Ausführungsform der Erfindung ist eine Emulsion,
welche als Schutzcreme oder -milch vorliegt und beispielsweise Fettalkohole,
Fettsäuren, Fettsäureester, insbesondere Triglyceride
von Fettsäuren, Lanolin, natürliche und synthetische Öle
oder Wachse und Emulgatoren in Anwesenheit von Wasser enthält.
-
Weitere
bevorzugte Ausführungsformen stellen ölige Lotionen
auf Basis von natürlichen oder synthetischen Ölen
und Wachsen, Lanolin, Fettsäureestern, insbesondere Triglyceriden
von Fettsäuren, oder ölig-alkoholische Lotionen
auf Basis eines Niedrigalkohols, wie Ethanol, oder eines Glycerols,
wie Propylenglykol, und/oder eines Polyols, wie Glycerin, und Ölen,
Wachsen und Fettsäureestern, wie Triglyceriden von Fettsäuren,
dar.
-
Die
Zubereitung kann auch als alkoholisches Gel vorliegen, welches einen
oder mehrere Niedrigalkohole oder -polyole, wie Ethanol, Propylenglykol
oder Glycerin, und ein Verdickungsmittel, wie Kieselerde umfasst.
Die ölig-alkoholischen Gele enthalten außerdem
natürliches oder synthetisches Öl oder Wachs.
-
Die
festen Stifte bestehen aus natürlichen oder synthetischen
Wachsen und Ölen, Fettalkoholen, Fettsäuren, Fettsäureestern,
Lanolin und anderen Fettkörpern.
-
Ist
eine Zubereitung als Aerosol konfektioniert, verwendet man in der
Regel die üblichen Treibmittel, wie Alkane, Fluoralkane
und Chlorfluoralkane, bevorzugt Alkane.
-
Die
einzusetzenden Zubereitungen können dabei mit Hilfe von
Techniken hergestellt werden, die dem Fachmann wohl bekannt sind.
-
Ein
Verfahren zur Herstellung einer erfindungsgemäßen
Zubereitung, wie zuvor beschrieben kann ein Vermischen des mindestens
einen α-Aminosäurederivats mit mindestens einer
schwerlöslichen Substanz und einem für topische
Anwendungen geeigneten Träger, beispielsweise einem kosmetisch,
pharmazeutisch oder dermatologisch geeigneten Träger, sein.
Das Vermischen kann ein Lösen, Emulgieren oder Dispergieren
in dem Träger zur Folge haben.
-
Auch
ohne weitere Ausführungen wird davon ausgegangen, dass
ein Fachmann die obige Beschreibung in weitestem Umfang nutzen kann.
Die bevorzugten Ausführungsformen und Beispiele sind deswegen lediglich
als beschreibende, keinesfalls als in irgendeiner Weise limitierende
Offenbarung aufzufassen. Die vollständige Offenbarung aller
vor- und nachstehend aufgeführten Anmeldungen und Veröffentlichungen
sind durch Bezugnahme in diese Anmeldung eingeführt.
-
Die
Gewichtsprozentverhältnisse der einzelnen Inhaltsstoffe
in den Zubereitungen der Beispiele gehören ausdrücklich
zur Offenbarung der Beschreibung und können daher als Merkmale
herangezogen werden.
-
Die
im folgenden angeführten Beispiele für den erfindungsgemäßen
Gegenstand dienen lediglich der Erläuterung und engen die
vorliegende Erfindung keineswegs in irgendeiner Weise ein. Im übrigen
ist die beschriebene Erfindung im gesamten beanspruchten Bereich
ausführbar. Alle Verbindungen oder Komponenten, die in
den Zubereitungen verwendet werden können, sind entweder
bekannt und käuflich erhältlich oder können
nach bekannten Methoden synthetisiert werden. Es werden die INCI-Namen
der verwendeten Rohstoffe angegeben (die INCI-Namen werden definitionsgemäß in
englischer Sprache angegeben).
-
Beispiele
-
Steigerung der Löslichkeiten
von Tilirosid und 5,7-Diydroxy-2-methylchromon:
-
Zunächst
werden jeweils 4%-ige Ectoinlösungen in Wasser sowie in
einem Wasser-Ethanol-Gemisch (3:1) angesetzt. Der zu lösende
Wirkstoff wird anschließend zu 1% bzw. 1,5% in beide Ectoinlösungen
eingearbeitet. Als Vergleich dienen die jeweiligen ectoinfreien
Ansätze. Die Bewertung der Löslichkeitsteigerung durch
Ectoin erfolgte visuell (klare Lösung in Kombination mit
Ectoin, trübe Lösungen in Abwesenheit von Ectoin).
| | Ethanol/Wasser
3:1 | 4%
Ectoin in Ethanol/Wasser 3:1 |
| Tilirosid,
1% | trübe
Lösung | klare
Lösung |
| 5,7-Dihydroxy-2-methylchromon, 1,5% | trübe
Lösung | klare
Lösung |
-
Steigerung der Löslichkeit von
Phenylbenzimidazolsulfonsäure (PBSA):
-
Es
werden zunächst je 4%ige wässrige Lösungen
von Ectoin, Kreatinin und Pyrrolidoncarbonsäure hergestellt.
Anschließend wird der Wirkstoff PBSA im Überschuss
in die Lösung eindispergiert. Der pH-Wert der Suspension
wird auf 4,6 eingestellt. Ungelöster Wirkstoff wird nach
1-stündigem Rühren abfiltriert. Der gelöste
Wirkstoffanteil wird per Hochleistungsflüssigchromatographie
bestimmt. Als Vergleich dient der Versuch ohne Lösungsvermittler.
Im Fall des Lösens von PBSA in wässriger Kreatininlösung
wird zusätzlich die Löslichkeit bei pH 5,7 ermittelt,
d. h. in diesem Fall wird nicht auf pH 4,6 zurückgestellt.
Phenylbenzimidazolsulfonsäure
(PBSA) Ergebnisse:
| Löslichkeit
von PSBA in Wasser (pH Wert der Dispersion auf 4,6 eingestellt): | 0,34 g/L |
| Löslichkeit
von PSBA in Wasser enthaltend 4% Ectoin (pH Wert der Dispersion auf
4,6 eingestellt): | 0,60 g/L |
| Löslichkeit
von PSBA in Wasser enthaltend 4% Kreatinin (pH Wert der Dispersion auf
4,6 eingestellt): | 0,94 g/L |
| Löslichkeit
von PSBA in Wasser enthaltend 4% Kreatinin (pH Wert der Dispersion 5,7): | 8,50 g/L |
| Löslichkeit
von PSBA in Wasser enthaltend 4% Pyrrolidoncarbonsäure
(pH Wert der Dispersion auf 4,6 eingestellt): | 0,34 g/L |
-
Beispiele
für kosmetische Rezepturen enthaltend verschiedene Mischung
M1, M2, M3, wie nachfolgend beschrieben:
| Beispielrezepturen
A bis G für kosmetische Emulsionen |
| | A | B | C | D | E | F | G |
| Glycerylstearat | 1 | 1 | 1 | 1 | 1 | 1 | 1 |
| Stearinsäure | 3 | 3 | 3 | 3 | 3 | 3 | 3 |
| Behenylalkohol | 2 | 2 | 2 | 2 | 2 | 2 | 2 |
| Cetylalcohol | 2 | 2 | 2 | 2 | 2 | 2 | 2 |
| Hydrierte
Kokosfettglyceride | 1 | 1 | 1 | 1 | 1 | 1 | 1 |
| C12-15
Alkylbenzoat | 2 | 2 | 2 | 2 | 2 | 2 | 2 |
| Octyldodecanol | 2 | 2 | 2 | 2 | 2 | 2 | 2 |
| Octamethyltetrasiloxan
(Cyclomethicon) | 2 | 2 | 2 | 2 | 2 | 2 | 2 |
| Dimethylpolysiloxan
(Dimethicon) | 1 | 1 | 1 | 1 | 1 | 1 | 1 |
| Dicaprylylcarbonat | 4 | 4 | 4 | 4 | 2 | 2 | 2 |
| Butylmethoxydibenzoylmethan | 1 | | | | 1 | 1 | 2 |
| Ethylhexylmethoxycinnamat | 2 | | 2 | | 4 | 4 | 6 |
| Titandioxid
(Eusolex T-Avo) | 0,5 | 1 | 1 | 2 | 0,5 | 1 | |
| Methylen
Bis-benzotriazolyl Tetramethylbutylphenol (Tinosorb® M) | | 3 | | | | | |
| Bis-Ethylhexyloxyphenol
Methoxyphenyl Triazin (Tinosorb® S) | | | 1 | 2 | | | |
| Bis-Ethylhexyl
Hydroxydimethoxy benzylmalonat (RonaCare® AP) | 0,5 | 1,0 | 2,0 | 0,5 | 1,5 | 0,25 | 1,5 |
| Ubichinon
(Q10) | 0,05 | | 0,05 | | 0,05 | | 0,05 |
| Panthenol | | 0,5 | | 0,5 | | 0,5 | |
| Mischung
M1 | 2 | 4 | 8 | | | | |
| Mischung
M2 | | | | 1 | 2 | | |
| Mischung
M3 | | | | | | 1 | 2 |
| Natriumascorbylphosphat | 0,3 | 0,3 | 0,3 | 0,3 | 0,3 | 0,3 | 0,3 |
| Tocopherylacetat | 0,5 | 0,5 | 0,5 | 0,5 | 0,5 | 0,5 | 0,5 |
| Iminodisuccinat | 0,2 | 0,2 | 0,2 | 0,2 | 0,2 | 0,2 | 0,2 |
| Phenoxyethanol | 0,3 | 0,3 | 0,3 | 0,3 | 0,3 | 0,3 | 0,3 |
| p-Hydroxybenzoesäurealkylester (Paraben) | 0,6 | 0,6 | 0,6 | 0,6 | 0,6 | 0,6 | 0,6 |
| Ethanol
denaturiert | 3 | 3 | 3 | 3 | 3 | 3 | 3 |
| Carrageenan | 0,1 | 0,1 | 0,1 | 0,1 | 0,1 | 0,1 | 0,1 |
| Polyacrylsäure
(Carbomer) | 0,1 | 0,2 | 0,3 | 0,05 | 0,1 | 0,05 | 0,1 |
| Glycerin | 7 | 5 | 3 | 5 | 5 | 5 | 5 |
| Parfüm | 0,5 | 0,5 | 0,5 | 0,5 | 0,5 | 0,5 | 0,5 |
| NaOH/Citronensäure | q. s. zur
Einstellungvon pH = 5,5 |
| Wasser | Ad
100 | Ad
100 | Ad
100 | Ad
100 | Ad
100 | Ad
100 | Ad
100 |
-
Beispiele für Mischungen M1,
M2, M3:
-
Mischung M1:
-
- Zusammensetzung in Gewichtsprozenten: 75% Kreatinin, 25%
PBSA
-
Herstellung:
-
30
g Kreatinin werden unter Rühren bei Raumtemperatur in 500
ml Wasser gelöst, anschließend werden 10 g PBSA
(Eusolex® 232) eingetragen. Die
Lösungsmittel werden im Vakuum (60 mbar) und einer Badtemperatur
von 50°C entfernt. Das weiße Feststoffgemisch
wird 48 h bei 200 mbar und 40°C im Trockenschrank nachgetrocknet
und anschließend gesiebt (100 μm Sieb).
-
Mischung M2
-
- Zusammensetzung in Gewichtsprozenten: 80% Ectoin, 20% Tilirosid
Herstellung:
-
30
g Ectoin werden unter Rühren bei Raumtemperatur in 500
ml Ethanol-Wassergemisch (3:1) gegeben. Anschließend werden
7,5 g Tilirosid eingetragen. Die Lösungsmittel werden im
Vakuum (60 mbar) und einer Badtemperatur von 50°C entfernt.
Das gelbe Feststoffgemisch wird 48 h bei 200 mbar und 40°C
im Trockenschrank nachgetrocknet und über ein 100 μm
Sieb gegeben. Als alternative Trockungsmethode kann das Ethanol/Wasser-Gemisch
auch sprühgetrocknet werden.
-
Mischung M3:
-
- Zusammensetzung in Gewichtsprozenten: 70% Kreatinin, 21%
Isoquercetin, 8,5% Kieselsäure
-
Herstellung:
-
25
g Kreatinin werden unter Rühren bei Raumtemperatur in 500
ml Ethanol-Wassergemisch (3:1) gegeben. Anschließend werden
7,5 g Isoquercetin eingetragen. Die Lösungsmittel werden
im Vakuum (60 mbar) und einer Badtemperatur von 50°C entfernt.
Das gelbe Feststoffgemisch wird mit 3 g Kieselsäure versetzt,
für 48 h bei 200 mbar und 40°C im Trockenschrank
nachgetrocknet und über ein 100 μm Sieb gegeben.
Alternativ zur Verwendung von Kieselsäure (z. B. Aerosile,
wie Aeroperl 300/30) können als alternative Trennmittel
Stärke, Talk oder Zinkoxid verwendet werden.
-
ZITATE ENTHALTEN IN DER BESCHREIBUNG
-
Diese Liste
der vom Anmelder aufgeführten Dokumente wurde automatisiert
erzeugt und ist ausschließlich zur besseren Information
des Lesers aufgenommen. Die Liste ist nicht Bestandteil der deutschen
Patent- bzw. Gebrauchsmusteranmeldung. Das DPMA übernimmt
keinerlei Haftung für etwaige Fehler oder Auslassungen.
-
Zitierte Patentliteratur
-
- - DE 4116123
A [0075]
- - DE 10244282 A [0081]
- - DE 10232595 A [0091]
- - US 6242099 B1 [0098]
- - WO 00/09652 [0098]
- - WO 00/72806 [0098]
- - WO 00/71084 [0098]
- - DE 10133202 A [0101, 0101]
- - DE 4308282 A [0131]